.
Краткая теоретическая часть
Первый закон термодинамики, являясь частным случаем общего закона сохранения и превращения энергии констатирует наличие процессов превращения видов энергии и ее сохранение, но не устанавливает условий, при которых эти превращения возможны.
Второй закон термодинамики устанавливает, что самопроизвольные процессы возможны лишь в том случае, когда в системе нет равновесия и что эти процессы всегда протекают в направлении, при котором система приближается к равновесному состоянию, т.е. он указывает направленность процесса.
Теплота и работа являются формами передачи энергии: первая, связанная с движением молекул и атомов – микроскопическая форма передачи энергии, а вторая, связанная с перемещением тела или его частей – макрофизической. Теплота и работа не являются равноценными формами передачи энергии.
Работа легко и полностью превращается в теплоту.
Превращение теплоты в работу, например, в тепловых машинах, происходит только при наличии разности температур между источником теплоты и теплоприемником, причем не вся теплота превращается в работу.
Все виды энергии в конечном счете превращаются в теплоту, которая затем рассеивается в окружающей среде. Мера этого рассеивания или обесценивания энергии называется энтропией.
Таким образом, для превращения теплоты в работу необходимо иметь два источника теплоты: один – с высокой температурой, а другой – с низкой температурой, и работа тепловой машины должна быть цикличной, т.е. рабочее тело, совершая ряд процессов должно возвращаться в исходное состояние.
Цикл, в результате которого получается положительная работа называется прямым циклом или циклом теплового двигателя; в нем работа расширения больше работы сжатия.
Циклы, в результате которых расходуется работа, называются обратными; в них работа сжатия больше работы расширения и они используются в холодильных установках и тепловых насосах.
Циклы тепловых машин характеризуются термическим коэффициентом:
 (1.1) (1.1)
а обратных циклов – коэффициентом эффективности:
 (1.3) (1.3)
 (1.4) (1.4)
Цикл, который позволяет получить наибольшие коэффициенты (см. формулы (1.1) – (1.3)), вошел в историю как цикл Карно и он состоит из двух изотерм и двух адиабат.
Задачи для самостоятельного решения.
Задача № 1-1. Машина, в цилиндре которой 1 кг воздуха, работает по циклу Карно в пределах температур Т1 = 523 К и Т2 = 303 К. Максимальное давление Р1 = 10 бар, а минимальное – Р2 = 1,2 бар. Определить параметры состояния воздуха в характерных точках цикла, количество подведенного и отведенного тепла, работу и термический КПД цикла.
Задача № 1-2. К газу в круговом процессе подведено 250 кДж тепла, а термический КПД цикла равен 0,46. Определить работу цикла.
Задача № 1-3. Сравните между собой два цикла, каждый из которых состоит из трех процессов: изотермического, адиабатного и изохорного (см. Рис.6.1).
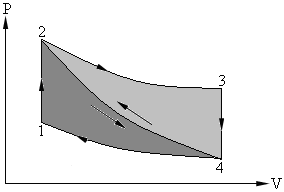
Рис. 1.1.
В первом цикле изотермический процесс осуществляется при максимальной температуре цикла, а во втором цикле – при минимальной температуре. Для обоих циклов: ТMAX = 900 К; ТMIN = 300 К; РMIN = 0,98 бар. Определить параметры (P, v, T, S) в характерных точках обоих циклов и их термические КПД. Рабочее тело в циклах – азот, теплоемкость которого принять постоянной. Изобразить циклы в T – S координатах.
Задача № 1-4. Определить изменения энтропии 3 кг азота в политропном процессе (n = 1,2), если температура азота изменилась от Т1 = 373 К до Т2 = 573 К. Изобразить процесс в P – V и T – S координатах.
Задача № 1-5. Определить термический КПД теплового двигателя, работающему по обратимому циклу Карно, если Т1 = 773 К, а Т2 = 298 К. Определить также количество подводимого и отводимого тепла, если мощность двигателя равна N = 5000 кВт.
Пример. Для идеального цикла газовой турбины с подводом тепла при P = Const определить параметры в характерных точках, полезную работу, термический КПД, количество подведенного и отведенного тепла, если дано: Р1 = 1 бар, t1 = 27 °C, t3 = 700 °C, β = Р2/Р1 = 10, k = 1,4, рабочее тело – воздух.
Решение.
V1 = R × T1/(μ × P1) = 8,314 × (27 + 273,15) /(2,896 × 10–2 × 105) = 0,862 м3/кг.
T2 = T1 × (Р2 /Р1) (k – 1) /k = T1 × β(k – 1) /k = (27 + 273,15) × 10(1,4 – 1) /1,4 = 579,50 K.
P2 = β × Р1 = 10 × 105 = 106 Па.
V2 = R × T2/(μ × P2) = 8,314 × 579,50/(2,896×10–2 × 106) = 0,166 м3/кг.
V3 = V2 × (T3/T2) = 0,166 × (700 + 273,15) /579,50 = 0,279 м3/кг.
T4 = (T3 × T1) /T2 = (700 + 273,15) × (27 + 273,15) /579,50 K = 504,04 K.
V4 = V1 × (T4/T1) = 0,862 × 504,04/(27 + 273,15) = 1,448 м3/кг.
q2–3 = CP × (T3 – T2) = 1,01 × ((700 + 273,15) – 579,50) = 397,59 кДж/кг.
q4–1 = CP × (T4 – T1) = 1,01 × (504,04 – (27 + 273,15)) = 205,93 кДж/кг.
l = q1 – q2 = 397,59 – 205,93 = 191,66 кДж/кг.
ηT = 1 – q2/q1 = 1 – 205,93/397,59 = 0,4821.
Задача № 1-6. Газовая турбина работает по циклу с подводом тепла при P = Const. Известны параметры: Р1 = 1 бар, t1 = 40 °C, t4 = 400 °C, β = 3; рабочее тело – воздух. Определить параметры в характерных точках цикла, количество подведенного и отведенного тепла, работу за цикл и термический КПД.
Задача № 1-7. Компрессор всасывает 400 м3/ч воздуха при давлении Р1 = 1 бар и температуре t1 = 20 °C и сжимает его до давления Р2 = 5 бар. Определить теоретическую работу компрессора при адиабатном сжатии и температуру воздуха в конце сжатия.
Задача № 1-8. Компрессор всасывает 100 м3/ч воздуха при давлении Р1 = 1 бар и температуре t1 = 27 °C. Конечное давление воздуха составляет Р2 = = 8 бар. Определить теоретическую мощность двигателя для привода компрессора и расход охлаждающей воды, если ее температура повышается на 13 °C. расчет произвести для изотермического, адиабатного и политропного (n = 1,2) сжатия.
Задача № 1-9. Холодильная установка, находящаяся в помещении с температурой 293 К, имеет холодопроизводительность 6000 ккал/ч и поддерживает в холодильной камере температуру 263 К. Приняв, что установка работает по обратимому циклу Карно, определить холодильный коэффициент, количество тепла Q, передаваемое окружающему воздуху, и теоретическую мощность привода установки.
Пример. В компрессор холодильной установки поступает воздух из камеры с давлением Р1 = 1 бар и температурой t1 = – 10 °C, где он адиабатически сжимается до давления Р2 = 5 бар (см. Рис.6.2). Температура воздуха в процессе P = Const снижается до t3 = 10 °C, затем он в цилиндре по адиабате 3 – 4 расширяется до давления Р4 = Р1, после чего поступает в камеру, в которой нагревается (процесс 4 – 1) до температуры t1 = – 10 °C.
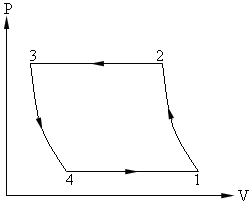
Рис. 1.2.
Определить температуру воздуха, поступающего в камеру, теоретическую работу цикла, холодопроизводительность воздуха и холодильный коэффициент для данной установки и для установки, работающей в том же интервале температур по циклу Карно.
Решение.
Т4 = Т3 × (Р4/Р3) (k – 1) /k = Т3 × (Р1/Р2) (k – 1) /k = (10 + 273,15) × (1/5) (1,4 – 1) /1,4 = 178,78 К.
Т2 = Т1 × (Р2/Р1) (k – 1) /k = (– 10 + 273,15) × (5/1) (1,4 – 1) /1,4 = 416,78 К.
lК = (k/(k – 1)) × (R/μ) × T1 × [(P2/P1) (k – 1) k – 1] = (1,4/(1,4 – 1)) × (8,314/2,896×10–2) × (– 10 + 273,15) × [(5/1) (1,4 – 1) /1,4 – 1] = 154,37 кДж/кг.
lРЦ = (k/(k – 1)) × (R/μ) × T3 × [(P4/P3) (k – 1) k – 1] = (1,4/(1,4 – 1)) × (8,314/2,896×10–2) × (10 + 273,15) × [(1/5) (1,4 – 1) /1,4 – 1] = – 104,87 кДж/кг.
l0 = lК – lРЦ = 154,37 – (– 104,87) = 259,24 кДж/кг;
Холодопроизводительность:
q0 = CP × (T1 – T4) = 1,0104 × ((– 10 + 273,15) – 178,78) = 85,25 кДж/кг.
Холодильный коэффициент данной установки:
εУ = q0/l0 = 85,25/259,24 = 0,33.
Работающей по циклу Карно:
εЦК = Т1/(Т3 – Т1) = (– 10 + 273,15) /((10 + 273,15) – (– 10 + 273,15)) = 13,16.
Задача № 1-10. Воздушная холодильная установка имеет холодопроизводительность Q = 200000 ккал/ч. Состояние воздуха, всасываемого компрессором, характеризуется давлением Р1 = 1 атм и температурой t1 = – 10 °C. Давление воздуха после сжатия Р2 = 4 атм, а его температура при поступлении в расширительный сосуд равна t3 = 20 °C. Определить теоретическую мощность двигателя компрессора и расширительного цилиндра, холодильный коэффициент установки, расход воздуха, а также количество тепла, передаваемого охлаждающей воде.
Задача № 1-11. Холодопроизводительность воздушной установки Q = 20000 ккал/ч. Определить ее холодильный коэффициент и теоретическую мощность двигателя, если известно, что максимальное давление в установке Р2 = 5 атм, минимальное – Р1 = 1,1 атм, температура воздуха в начале сжатия t1 = 0 °C, а при выходе из охладителя t3 = 20 °C. Сжатие и расширение воздуха принять политропным (n = 1,28).
Задача № 1-12. Определить эксергию воздуха в баллоне при Р = 150 бар и параметрах окружающего воздуха в помещении, которые равны Р0 = 1 бар, Т0 = 293 К. Объем воздуха в баллоне 40 дм3.
Задача № 1-13. Определить эксергию азота, находящегося в пьезометре экспериментальной установки при параметрах Р = 250 бар и Т = 973 К. Параметры окружающей среды Р0 = 1 бар и Т0 = 293 К. Объем азота в пьезометре 500 см3. Азот считать идеальным газом.
Пример. Камень массой m = 1,2 кг падает с высоты Н = 14 м на землю. Определить вызванное этим процессом изменение энтропии системы камень-земля. Температура камня и окружающей среды равна Т = 293 К.
Решение. Изменение энтропии системы в данном необратимом процессе, вычисляется как потеря работоспособности, равная убыли потенциальной энергии, то есть L = T0 × ΔS = M × ΔH. Отсюда:
ΔS = m × g × H/T0 = 1,2 × 9,81 × 14/293 = 0,562 Дж/(кг×К).
Задача № 1-14. Определить эксергию 100 кДж тепла при температуре 973 К. Температура среды 273 К. Определить потерю энергии этого тепла, если оно будет передано тепловому источнику с температурой 273 К.
Пример. В цикле рабочее тело (гелий; СP = 5,19 кДж/(кг×К)) получает тепло, изобарически (P = Const) нагреваясь от t1 = 300 °C до t2 = 850 °C. Термический КПД цикла ηT = 0,33, температура окружающей среды t0 = 25 °C. Определить эксергетический КПД и потери эксергии цикла.
Решение.
Подведенное тепло составляет:
q = h2 – h1 = CP × (t2 – t1) = 5,19 × (850 – 300) = 2854,5 кДж/кг.
Эксергию тепла находим:

Энергия тепла будет:
 
и, следовательно,
lq = q – bq = 2854,5 – 1041,0 = 1813,5 кДж/кг.
Так как lq – максимально полезная работа, получаемая из тепла, то из уравнения термического КПД получаем:
– lT = ηT × q = 0,33 × 2854,5 = 942,0 кДж/кг.
Эксергетический КПД находим как:
ηЭ = – lT/lq= 942,0/1813,5 = 0,52.
Потери эксергии в цикле получим:
dЭ = (1 – ηЭ) × lq = (1 – 0,52) × 1813,5 = 870,5 кДж/кг.
Подлинные потери выражаются именно этой величиной, а не общим теплоотводом:
|q0| = q + lT = 2854,5 – 942,0 = 1912,5 кДж/кг
потому что здесь на виду с принципиально устранимыми потерями эксергии dЭ содержится также ни при каких обстоятельствах не превращаемая в работу энергия bq подведенного тепла
|q0| = bq+ dЭ = 1041,0 + 870,5 = 1911,5 кДж/кг.
Пример. Определить эксергию тепла, которое выделяется при сгорании на воздухе 1 кг топлива с теплотой сгорания QPН = 20000 кДж/кг. Температура горения 1573 К. Давление среды Р0 = 1 бар, Т0 = 293 К. Теплоемкость продуктов сгорания принять постоянной.
Решение. Источник в процессе превращения тепла в работу будет охлаждаться. Поэтому его температура будет переменна. Когда температура источника станет равной температуре среды, его работоспособность будет исчерпана.
Процесс охлаждения источника (линия 1 – 0) показан на рис. №6.3.
Для бесконечно малого количества тепла dQ при температуре Т дифференциал эксергии определяется через термический КПД цикла Карно:
dlX = dQ × (1 – T0/T1)
и тогда эксергия находится как:

Величина эксергии численно равна выделенной площади, изображенной на Рис. 1.3.
Величина Q2 = T0 × (S1 – S2) равна тому количеству тепла, которое надо передать нижнему источнику (среде) в процессе превращения тепла в работу.

Рис. 1.3
Изменение энтропии определяется как:
S1 – S2 = Cm × ln(T1/T2),
где Cm – теплоемкость источника тепла, которая равна:
Cm = Q/(T1 – T0).
С учетом написанных соотношений, эксергию тепла находим как:
lX = Q – T0 × [Q/(T1 – T0)] × ln(T1/T0) = Q × (1 – [T0/(T1 – T0)] × ln(T1/T0)) = = 20000 × (1 – [293/(1573 – 293)] × ln(1573/293)) = 12 МДж.
Задача № 1-15. В проточном теплообменнике нагревается воздух, имеющий на входе Р1 = 7 бар, Т1 = 213 К, а на выходе Р2 = 0,3 бар, Т2 = 1073 К. Параметры среды Р0 = 1 бар, Т0 = 288 К. Определить изменение эксергии 1 кг воздуха в теплообменнике, считая воздух идеальным газом.
Задача № 1-16. Построить в P – v и T – S координатах циклы и исследовать их: определить знак изменения внутренней энергии, энтальпии, энтропии, теплоемкости, работы и тепла в каждом процессе, если цикл состоит из следующих процессов с показателем политропы n:
а) расширение (n = 0,5); б) сжатия (n = – 475); в) сжатие (n = 7,5).
а) сжатие (n = 150); б) расширение (n = 0,8); в) сжатие (n = – 15).
а) расширение (n = 0); б) расширение (n = 1); в) расширение (n = 0); г) нагревание (n = ¥); д) сжатие (n = 0).
а) сжатие (n = 0,5); б) расширение (n = – 1); в) расширение (n = 5).
а) расширение (n = 1,1); б) сжатие (n = 0); в) расширение (n = – 2).
а) охлаждение (n = ¥); б) расширение (n = – 3); в) сжатие (n = 0,8).
а) расширение (n = 230); б) расширение (n = – 1); в) сжатие (n = 1,1).
а) расширение (n = 0); б) сжатие (n = – 1,5); в) сжатие (n = 17).
Для построения циклов использовать обобщенные зависимости политропных процессов в P – v и T – S координатах.
Пример. Построить цикл: а) расширение (n = 0); б) сжатие (n = – 1,5); в) сжатие (n = 17).
Решение. Процесс расширения n = 0 расположен на P – v диаграмме (ΔV > 0) правее изохоры и совпадает с линией n =0; процесс сжатия n = – 1,5 (ΔV < 0 и ΔP < 0) находятся в IV квадранте между линиями n = – 1 и n = – ∞; процесс сжатия n = 17 (ΔV < 0, ΔP > 0) расположен в I квадранте между линиями n = kи n = + ∞. Эти процессы в T – S координатах располагаются соответственно показателям политропы с учетом их значений, а также знаков "+" или "–" изменений температуры и энтропии: процесс "а" – во II квадранте, так как в P – v координатах он лежит выше изотермы (n = 1, и ΔТ = 0) и адиабаты (n = k; ΔS = 0); процесс "б" располагается в IV квадранте между линиями n = k и n = + ∞.
Изобразим эти линии в координатах P – V и T – S в виде замкнутых циклов, сохраняя последовательность и направленность процессов (см. Рис. 1.4).
Знак изменения термодинамических функций состояния и процесса определяется из основных соотношений первого и второго законов термодинамики:
Δu = CVΔT; (6.5)
Δh = CPΔT; (6.6)
 (1.7) (1.7)

Рис. 1.4
 (6.8) (6.8)
 (6.9) (6.9)
Результаты исследования занесём в таблицу.
Таблица № 1.1.
| Процесс |
Величина |
| ΔP |
ΔV |
ΔT |
Δu |
Δh |
Δs |
C |
q |
l |
| n = 0 (расширение) |
0 |
>0 |
>0 |
>0 |
>0 |
>0 |
>0 |
>0 |
>0 |
| n = – 1,5 (сжатие) |
<0 |
<0 |
<0 |
<0 |
<0 |
<0 |
>0 |
<0 |
<0 |
| n = 17 (сжатие) |
>0 |
>0 |
>0 |
>0 |
>0 |
>0 |
>0 |
>0 |
<0 |
Исследование процессов получения сжатого газа в компрессорах.
Краткая теоретическая часть
Задачей термодинамического анализа процессов, происходящих в компрессоре, является определение оптимальной работы, которую необходимо затратить для получения единицы сжатого газа при заданных начальных и конечных параметрах газа и, как следствие, мощности электрического двигателя.
В качестве примера рассмотрим поршневой компрессор (см. рис.7.1), который состоит из цилиндра с охлаждающей рубашкой 1, поршня 2, всасывающего 3 и нагнетательного 4 клапанов и холодильника 5.
При возвратно-поступательном движении поршня 2 происходит всасывание газа процесс 0–1, сжатие его – процесс 1–2 и выталкивание – процесс 2–3 (см. рис.7.2).
Удельная техническая работа одноступенчатого компрессора при определенных допущениях может быть рассчитана как:
 (2.1) (2.1)

Рис. 2.1.

Рис. 2.2.
Величина работы во многом зависит от процесса сжатия 1–2 (T = Const, S = Const, n = Const) и для политропного процесса с показателем политропы 1 < n < kрассчитывается как (по знаку она будет отрицательной):
 (7.2) (7.2)
В процессе сжатия при n = Const необходимо от сжимаемого газа через рубашку цилиндра отводить тепло, которое рассчитывается как:
qn = Cn(t2 – t1) (7.3)
Чтобы сжатый газ можно было бы использовать в практике его необходимо охладить в холодильнике 5 при P = Const (см. рис.7.1).
qP = CP(t1 – t2) (7.4)
В реальных условиях процесс сжатия лимитируется наличием "вредного" пространства в цилиндре и процессами, происходящими в нем. Так, при степени сжатия газа β = P2/P1 ≈ 29 производительность компрессора будет равна нулю. Поэтому, при одноступенчатом сжатии газа в реальных условиях принимают β = P2/P1 ≈ 5 ÷ 7.
Для сжатия газа до более высоких давлений применяют многоступенчатые компрессоры (см. рис.7.3) которые представляют собой соединенные последовательно одноступенчатые компрессоры.

Рис. 2.3
Из условий минимальной работы двухступенчатого компрессора вытекает, что степени сжатия каждой ступени β равны, Р2/Р1 = Р3/Р2 и так далее. Из этого также следует, что при условии P1 = 1 бар, степень сжатия газа в многоступенчатом компрессоре β при числе ступеней Z, будет определяться как:
 (7.5) (7.5)
и работа при сжатии единицы газа в каждой ступени компрессора будет одинаковой, то есть:
l1 = l2 = … = ln. (7.6)
Соотношения между параметрами (P, v, T) сжимаемого газа, а также расчет изменения внутренней энергии, энтальпии и энтропии с учетом формулы (7.5) определяются по формулам, приведенным в таблицах №5.1 – №5.3.
Количество теплоты, отводимое от газа в процессе сжатия через "рубашки" цилиндра рассчитывается по формуле (7.3), а в холодильнике – (7.4).
С учетом количества сжимаемого газа M теплота и работа при многоступенчатом сжатии рассчитываются как:
Q = MZ(qn + qP); (7.7)
L = MZl. (7.8)
Количество холодильного агента MХА, используемого для охлаждения сжимаемого газа, рассчитывается из уравнения теплового баланса:
 (7.9) (7.9)
Мощность электрического двигателя компрессора рассчитывается по формуле:
 (7.10) (7.10)
Пример. Произвести термодинамический расчет процессов в двухступенчатом компрессоре при политропном (n = 1,2) сжатии. V1 = 35 м3/мин воздуха от начальных условий P1 = РНАЧ = 105 Н/м2, t1 = 15 °Cдо конечных P5 = РКОН = 45 × 105 Н/м2, t5 = 15 °C. Теплоемкости воздуха CV = 0,72 кДж/(кг×К), CP = 1,005 кДж/(кг×К). Охлаждающем агентом принять воду (СP = 4,19 кДж/(кг×К)), температура которой на входе равна tВХ = 10 °C, а на выходе tВЫХ = 25 °C. Коэффициент эффективности принять равным ηЭФФ = 0,7.
Расчет параметров состояния газа (P, V, T) с учетом формулы (7.5) и изменения функций состояния, а также расчёт функций процесса производим по формулам (см. таблицы №5.1 – №5.3). Некоторые их значения приведены в таблицах №7.1 – №7.2 и графически на рисунке 7.4.
Таблица № 2.1.
| Точка |
T, К |
P × 10–5, Н/м2 |
V, м3/мин |
| 1 |
288,15 |
1,00 |
35,00 |
| 2 |
395,53 |
6,71 |
7,16 |
| 3 |
288,15 |
6,71 |
5,22 |
| 4 |
395,53 |
45,00 |
1,07 |
| 5 |
288,15 |
45,00 |
0,78 |
Таблица № 2.2.
| Процесс |
Δu, кДж/кг |
Δh, кДж/кг |
Δs, кДж/(кг×К) |
| 1-2 |
77,31 |
107,92 |
– 0,23 |
| 2-3 |
– 77,31 |
– 107,92 |
– 0,32 |
| 3-4 |
77,31 |
107,92 |
– 0,23 |
| 4-5 |
– 77,31 |
– 107,92 |
– 0,32 |
Масса воздуха равна:

Работа, затрачиваемая на сжатие воздуха в одной ступени компрессора равна:


Количество тепла, согласно формуле (7.7):



Процессы, происходящие в компрессоре в P – V и T – S координатах представлены на рисунке ниже.

Рис. 2.4.
|