Міністерство освіти і науки України
Чернігівський державний педагогічний університет імені Т.Г. Шевченка
Хіміко-біологічний факультет
КУРСОВА РОБОТА
Окисно-відновні реакції – основа біохімічних процесів в організмі людини
Чернігів – 2006
Вступ
За зміною ступеня окиснення елементів, які входять до складу вихідних речовин та продуктів реакції, хімічні реакції можна поділити на дві групи.
До першої групи належать реакції, що відбуваються без зміни ступенів окиснення елементів. Це реакції подвійного обміну, або витіснення, комплексоутворення, деякі реакції розкладу, реакції ізомеризації, полімеризації, асоціації тощо:
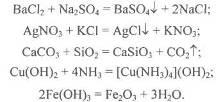
До другої групи належать реакції, що відбуваються із зміною ступенів окиснення елементів реагуючих речовин та продуктів реакції. Такі реакції називаються окисно-відновними,
наприклад:
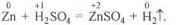
У процесі цієї реакції ступінь окиснення Цинку змінюється від 0 до +2, а Гідрогену – від +1 до 0. Отже, це окисно-відновна реакція.
Речовини, до складу молекул яких входять атоми, здатні приєднувати електрони, тобто знижувати свій ступінь окиснення, називаються окисниками.
Речовини, до складу молекул яких входять атоми, здатні віддавати електрони, тобто підвищувати свій ступінь окиснення, називаються відновниками.
Речовини, що містять у своєму складі елементи з проміжним ступенем окиснення, можуть бути як окисниками (у разі взаємодії з активнішим, ніж вони, відновником), так і відновниками (у разі взаємодії з активнішим, ніж вони, окисником).
Процеси окиснення завжди супроводжуються процесами відновлення. Один процес не може відбуватися без другого, оскільки вони пов'язані лише з переміщенням матеріальних частинок – електронів, а не з їх знищенням або створенням. Процес віддавання електронів, що супроводжується підвищенням ступеня окиснення елемента, називається окисненням.
Процес приєднання електронів, що супроводжується зниженням ступеня окиснення елемента, називається відновленням.
На процес окиснення – відновлення значною мірою впливають концентрації окисника і відновника. Із збільшенням концентрації окисника або зменшенням концентрації відновника окиснювальна здатність окисника зростає.
Можливість і характер перебігу окисно-відновного процесу іноді залежить від реакції середовища. Наприклад, у кислому середовищі сильний окисник перманганат-іон МnО4
–
відновлюється до Мn2+
, у лужному – йони Мангану Мn виступають як відновники, окиснюючись до Мn+4
(інколи до Мn+6
). У нейтральному і слабколужному середовищах як у процесі окиснення, так і в процесі відновлення сполук Мангану утворюється тетрагідроксид Мангану – Мn(ОН)4
. У сильнолужному середовищі сполуки Мангану окислюються та відновлюються до манганат-іона МnО4
-2
.
Окисно-відновні реакції мають величезне значення, особливо для підтримування життєдіяльності біологічних систем. Процеси фотосинтезу, дихання, травлення – все це ланцюги окисно-відновних реакцій.
Мета роботи:
з’ясувати особливості окисно-відновних реакцій в організмі людини.
Задачі:
- Розглянути відмінність окисно-відновних реакцій в живій та неживій природі.
- Встановити взаємозв’язок енергетичного та пластичного обміну.
Обмін речовин і енергії є однією з найважливіших і найсуттєвіших ознак живого організму. Живі організми – відкриті системи, для існування яких необхідний постійний двосторонній зв'язок (обмін) з навколишнім середовищем. З навколишнього середовища вони одержують поживні речовини та енергію, перетворюють їх, видозмінюють, використовуючи утворені сполуки для власних потреб, та повертають в навколишнє середовище кінцеві продукти обміну. Вся сукупність процесів поглинання, засвоєння речовин з навколишнього середовища та утворення і виділення кінцевих продуктів – суть обміну речовин.
Розглядаючи життя як вищу форму руху живої матерії, як спосіб існування біополімерних тіл та систем, здатних до самооновлення і самовідтворення в умовах постійного взаємозв'язку з навколишнім середовищем, незаперечним є те, що обмін речовин є основою всіх проявів життєдіяльності. Припинення обміну речовин рівнозначне припиненню життя. Обмін речовин відбувається і в неживій природі, однак цей процес значно відрізняється від обміну в живих системах. Ця відмінність зумовлена насамперед тим, що обмін речовин у живих організмах забезпечує постійне самооновлення та самовідтворення його складових частин і здійснюється завдяки злагодженій дії численних систем та специфічних факторів, що забезпечують процеси життєдіяльності. У неживій природі обмін відбувається в одному напрямі, що призводить до видозміни, а часто і руйнування неживих тіл. Оскільки обмін речовин між організмом та навколишнім середовищем зумовлює всі прояви життєдіяльності, його можна розглядати як своєрідну норму реагування організму на зміну умов середовища, тобто в процесі еволюції в живих організмах виникли і вдосконалились специфічні функції, що забезпечили виживання та їх розвиток. Отже, обмін речовин в живих організмах має багато суттєвих ознак. Насамперед для обміну речовин у живих організмах характерним є скоординованість біохімічних перетворень у просторі і часі, завдяки чому різні процеси, інколи прямо протилежні, здійснюються одночасно, не заважаючи один одному. Це значною мірою забезпечується за рахунок кампартменізації – окремі біохімічні перетворення відбуваються на певних ділянках клітин чи в специфічних органелах клітин. Досить важливим є і те, що перебіг процесів проходить у суворо визначеній послідовності, при цьому кожна попередня реакція створює умови для здійснення наступної. В цьому важлива роль належить біологічним каталізаторам – ферментам, які мають багато специфічних властивостей і забезпечують складні біохімічні перетворення численних субстратів та спряженість цих перетворень на метаболічному та енергетичному рівнях. Це створює умови для забезпечення саморегуляції та підтримання гомеостазу – необхідної умови існування живих організмів. [2, с. 322–325]
Вуглеводи займають дуже важливе місце в харчуванні людини і тварин. Вони складають більшу частину харчового раціону людини і є основним джерелом енергії.
Джерелом вуглеводів для людини є продукти рослинного походження – мука, крупи, картопля. Основним вуглеводом їх є крохмаль. З фруктами, ягодами і харчовими цукрами людина одержує переважно сахарозу і фруктозу.
Полісахариди, що надходять із їжею, попередньо підлягають розщепленню в травному каналі під дією певних ферментів. У результаті розщеплення утворюються моносахариди, які потім легко асимілюються тканинами організму.
Перетворення вуглеводів, головним чином глюкози, у тканинах людини і вищих тварин може відбуватися двома шляхами – анаеробним і аеробним.
Найпростішим шляхом окиснення органічних речовин, в основному вуглеводів, є бродіння – окиснення глюкози у безкисневому середовищі, тобто в анаеробних умовах. Акцептором електронів у цьому процесі виступає органічна молекула, що утворюється під час самого бродіння. Тому з хімічної точки зору бродіння – внутрішній окисно-відновний процес.
Найбільш важливу роль відіграють два тісно пов'язані між собою процеси.
1. Молочнокисле бродіння,
при якому з молекули глюкози як кінцевий продукт утворюються дві молекули молочної кислоти. Молочнокисле бродіння звичайно називають гліколізом.
2. Спиртове бродіння
супроводжується розщепленням молекули глюкози на дві молекули етилового спирту і дві молекули оксиду вуглецю (IV) СО2
.
Гліколіз і глікогеноліз.
Механізм цих процесів на цей час добре вивчений. Встановлено послідовність окремих стадій, виділено в чистому вигляді ферменти, установлені пункти окиснення і спряжене з ними фосфорилювання АДФ з утворенням АТФ, та енергетика цих процесів.
Гліколіз складається з двох стадій.
Перша стадія гліколізу характеризується утворенням тріозофосфорних ефірів. На цій стадії не відбувається ніяких окислювальних реакцій і не виділяється енергія.
Друга стадія гліколізу починається реакцією окиснення гліцеральдегід-3-фосфату. Ця реакція є одним з найбільш важливих етапів гліколізу, оскільки в результаті окиснення альдегідної групи гліцеральдегід-3-фосфату звільняється енергія, що зберігається у формі високоенергетичного окисненого продукту цієї реакції 1,3-дифосфогліцерату. Процес окиснення гліцеральдегід-3-фосфату й утворення АТФ складається з декількох етапів.
Спочатку:

Утворена при цьому нестійка макроергічна сполука взаємодіє з фосфатною кислотою:
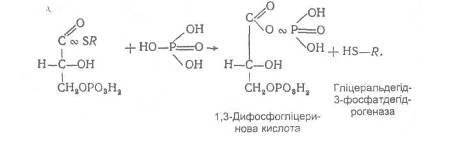
У результаті цієї реакції енергія карбоксил-тіолового макроергічного зв'язку зосереджується в карбоксил-фосфатному макроергічному зв'язку 1,3-дифосфогліцеринової кислоти, потім передається на фосфатну кислоту, унаслідок чого вона стає активованою і здатна вступати в реакцію фосфорилювання АДФ з утворенням АТФ. Такий механізм утворення АТФ носить назву субстратного фосфорилювання,
або фосфорилювання:
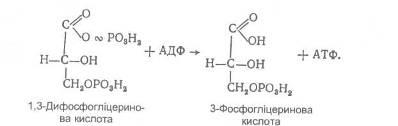
За допомогою ферменту фосфогліцеромутази
3-фосфогліцеринова кислота перетворюється у 2-фосфогліцеринову:

яка під дією енолази
втрачає молекулу води, перетворюється у фосфоенолпіруват. Це друга реакція в процесі гліколізу, у результаті якої утворюється високоенергетичний зв'язок. Відщеплення молекули води – це внутрішньомолекулярний окисно-відновний процес, що супроводжується перерозподілом енергії всередині молекули.
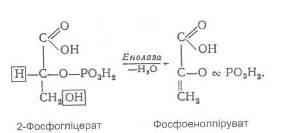
Під дією піруваткінази
залишок активованої фосфатної кислоти переноситься від фосфоенолпірувату на АДФ з утворенням АТФ і піровиноградної кислоти, тобто здійснюється друга реакція фосфорилювання АДФ на рівні субстрату:
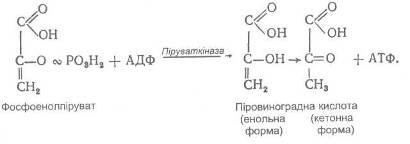
Завершальною реакцією усього процесу гліколізу є відновлення піровиноградної кислоти до молочної під дієюлактатдегідрогенази
:
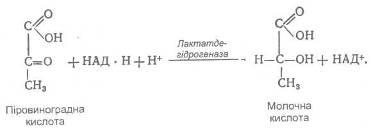
Утворенням молочної кислоти завершується друга стадія гліколізу, а водночас і весь процес перетворення глюкози в анаеробних умовах.
Анаеробне окиснення вуглеводів має ряд характерних рис. По-перше, воно відбувається багатоступінчато. Це забезпечує поступове звільнення енергії субстратами і її засвоєння. По-друге, енергія, що звільняється в процесі гліколізу, використовується не безпосередньо для тих або інших процесів, а запасається спочатку в макроергічних фосфатних зв'язках молекул АТФ. І, по-третє, активування неорганічної фосфатної кислоти і реакція фосфорилювання АДФ з утворенням АТФ здійснюються за рахунок енергії внутрішнього окисно-відновного процесу гліколізу. Таким чином, ці реакції свідчать про те, що гліколіз як один із видів бродіння являє собою внутрішній окисно-відновний процес.
Аналогічним способом і за участі тих же ферментів відбувається і спиртове бродіння.
Виняток становлять тільки останні дві реакції: піровиноградна кислота під дією піруватдекарбоксилази перетворюється в оцтовий альдегід, який під впливом відновленого коферменту НАД • Н + Н+
і алкогольдегідрогенази відновлюється до етилового спирту:
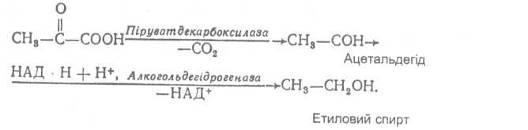
Як вихідна речовина для молочнокислого бродіння може використовуватися глікоген. У цьому випадку анаеробне окиснення називають глікогенолізом.
Дихання.
Аеробне окиснення вуглеводів відбувається за участі кисню повітря, тому його часто називають диханням. На відміну від гліколізу (глікогенолізу), при диханні роль акцептора виконує кисень.
Дихання, як і гліколіз, супроводжується утворенням однакових ефірів, фосфатів, а також проміжних продуктів. Багато реакцій гліколізу і дихання каталізуються тими самими ферментами. Іншими словами, при диханні перетворення глюкози до молочної кислоти проходить усі ті етапи, що і при гліколізі. Проте при цьому атоми водню, відщеплені від гліцеральдегід-3-фосфату, не відновлюють піровиноградну кислоту, а передаються на кисень, подолавши складну систему ферментів дихального ланцюга.
Перетворення молочної кислоти.
Утворена в анаеробних умовах при окисненні глюкози, молочна кислота окиснюється до СО2
і Н2
О в такий спосіб. Спочатку під дією ферменту лактатдегідрогенази,
коферментом якої є НАД+
, вона окислюється до піровиноградної кислоти:
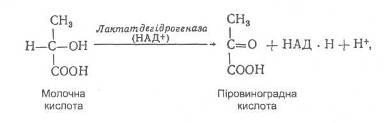
остання під впливом складного поліферментного комплексу, піддається окиснювальному декарбоксилюванню з утворенням активної форми оцтової кислоти – ацетил-КоА:
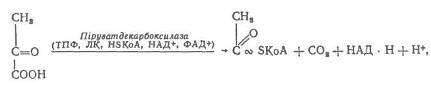
де ТПФ – тіамінпірофосфат; ЛК – ліпоєва кислота; НЗКоА – коензим А.
Перетворення піровиноградної кислоти в ацетил-КоА є перехідною стадією, завдяки якій вуглеводи включаються в новий етап – кисневе окиснення. Цей процес – сполучна ланка між гліколізом і власне диханням.
Цикл трикарбонових кислот (цикл
Кребса)
являє собою більш досконалий механізм окиснення вуглеводів, вироблений живими організмами з появою на Землі кисню. За допомогою цього механізму відбувається подальше перетворення оцтової кислоти у формі ацетил-КоА до СО2
і Н2
О. Першою реакцією циклу є реакція конденсації ацетил-КоА з щавлево-оцтовою кислотою, яку каталізує фермент цитрат-синтаза.
У результаті утворюється активна форма лимонної кислоти – цитрил-КоА:
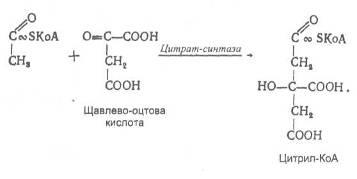
Гідролізуючись, цитрил-КоА перетворюється в лимонну кислоту:
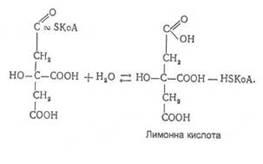
Остання під дією ферменту аконітатгідратази
перетворюється в цис-аконітову кислоту, яка, приєднуючи воду, перетворюється в ізолимонну кислоту:
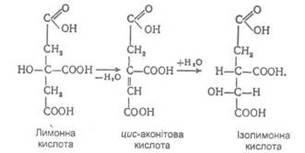
Ізолимонна кислота далі окислюється шляхом відщеплення двох атомів водню, перетворюючись у щавлево-янтарну. Щавлево-янтарна кислота, декарбоксилюючись, перетворюється в α-кетоглутарову кислоту НАД+
:
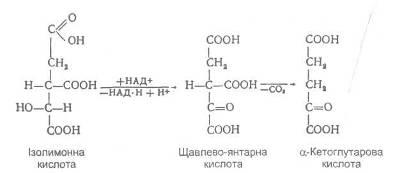
Наступним етапом циклу трикарбонових кислот є реакція окислювального декарбоксилювання α-кетоглутарової кислоти, у результаті якої утворюється янтарна кислота. Цей процес здійснюється у дві стадії. Перша стадія:
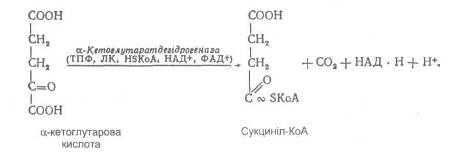
Друга стадія:

Утворений у результаті цієї реакції ГТФ взаємодіє з АДФ, утворюючи АТФ:
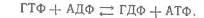
Надалі в ході циклу трикарбонових кислот відбувається ще два дегідрування.
Регенерована щавлево-оцтова кислота може знову вступати в реакцію з новою молекулою ацетил-КоА, і процес почнеться в тому ж порядку.
Загальну схему циклу трикарбонових кислот можна представити таким чином:
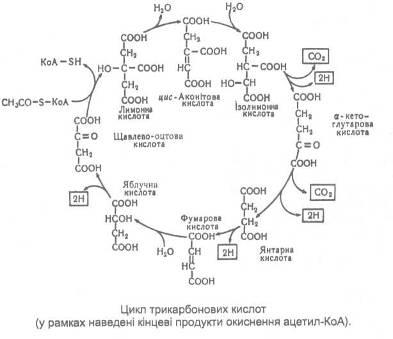
З даної схеми видно, що основна функція циклу Кребса полягає в дегідруванні оцтової кислоти.
Сумарна реакція цього циклу описується таким рівнянням:

із якого випливає, що чотири атоми водню належать воді. Отже, інші чотири утворилися при дегідруванні оцтової кислоти. Одночасно з цим у вигляді оксиду вуглецю (IV) двічі виділилося два атоми вуглецю тобто саме стільки, скільки їх надійшло в цикл у формі ацетильної групи.
Біосинтез вуглеводів.
Існує два основні шляхи біосинтезу вуглеводів із відносно нескладних метаболітів. Перший полягає у відновленні вуглекислого газу до глюкози. Він характерний для зелених рослин і названий фотосинтезом,
здійснюється за рахунок енергії сонячних променів за допомогою хлорофілу згідно з рівнянням:

У печінці, нирках і скелетних м'язах людини і вищих тварин існує інший шлях біосинтезу вуглеводів, який називають глюконеогенезом.
Глюконеогенез – це шлях, обернений гліколізу. Проте цей шлях має три стадії, що в енергетичному відношенні не можуть бути використані при перетворенні піровиноградної кислоти в глюкозу. Ці три стадії гліколізу замінені «обхідними» реакціями з меншою витратою енергії.
Першою обхідною реакцією є перетворення піровиноградної кислоти у фосфоенолпіровиноградну:


Далі відбувається ціла серія обернених реакцій, які закінчуються утворенням фруктозо – 1,6-дифосфату. Перетворення фруктозо – 1,6-дифосфату у фруктозо-6-фосфат – друга незворотна реакція гліколізу.
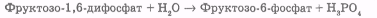
На наступній (оборотній) стадії біосинтезу глюкози фруктозо-6-фосфат перетворюється в глюкозо-6-фосфат під дією фосфоглюкоізомерази
гліколізу.
Розщеплення глюкозо-6-фосфату до глюкози – третя незворотна реакція, яка не здійснюється шляхом обернення гексокіназою.
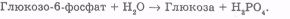
У більшості клітин глюкозо-6-фосфат, який утворюється в процесі глікогенолізу, використовується як попередник для біосинтезу оліго- і полісахаридів. Велику роль у біосинтезі цих складних сахаридів відіграє сполука уридиндифосфоглюкоза,
яка виконує роль проміжного переносника глюкози.
Розщеплення тригліцеридів. Одним з досить важливих етапів використання тригліцеридів у тканинах організму є розщеплення їх на складові частини – гліцерин і вищі жирні кислоти. Процес проходить за участю тканинних ліпаз. Перетворення гліцерину і жирних кислот протікає різними шляхами, що видно з наведеної схеми:
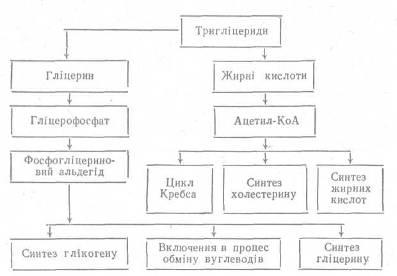
Окислення гліцерину.
Як видно з наведеної схеми, гліцерин, незалежно від дальшого використання у тканинах організму, насамперед піддається реакції фосфорилювання за участю АТФ при каталітичній дії ферменту гліцераткінази:
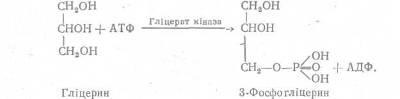
Найінтенсивніше цей процес проходить у клітинах печінки. Далі утворений 3-фосфогліцерин окислюється в тканинах до 3-фосфодіоксіацетону. Реакцію каталізує фермент гліцерофосфатдегідрогеназа:

З-Фосфодіоксіацетон, що утворився, ізомеризується в 3-фосфогліцериновий альдегід, який далі вступає в процеси перетворення, властиві для вуглеводів.
Окислення насичених жирних кислот.
Оскільки процес окислення жирних кислот розпочинається від вуглецевого атома, який знаходиться в β-положенні й окислюється в найбільшій мірі, він дістав назву β-окислення.
Так, було встановлено, що процес β-окислення жирних кислот здійснюється лише після активації їх специфічними ферментами, що містять у вигляді коферменту КоА–SH, який за участю сульфгідрильної групи утворює з жирними кислотами тіоефіри.
Процес β-окислення відбувається у мітохондріях клітин різних органів печінки, нирок, серцевого м'яза, скелетних м'язів тощо. Він включає такі основні етапи: активацію жирних кислот за участю АТФ і утворення тіоефірів КоА; β-окислення тіоефірів ацил-КоА, що утворились шляхом послідовного відщеплення атомів водню від алкільного ланцюга і відсікання двовуглецевих фрагментів у вигляді ацетил-КоА; окислення молекул ацетил-КоА в циклі Кребса до СО2
і Н2
О.
Активація жирних кислот є енергозалежним процесом, що здійснюється за рахунок енергії АТФ. Спочатку за участю ферменту аденілаткінази і АТФ утворюється ациладенілат:
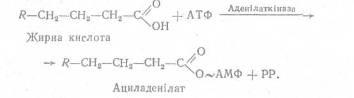
Далі ациладенілат взаємодіє з коензимом А. При цьому утворюється активна форма жирної кислоти – ацил-КоА.
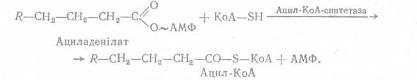
Процес активації жирних кислот є ключовою реакцією, підготовкою жирних кислот до всіх наступних перетворень.
Завдяки численним експериментальним дослідженням було встановлено, що крім β-окислення жирних кислот існує інший, другорядний шлях їх перетворення, який відбувається в цитоплазмі. Це, зокрема, процес α-окислення. Проміжними продуктами даного процесу є α-оксикислоти і α-кетокислоти, які далі перетворюються на жирні кислоти з непарною кількістю атомів вуглецю. В процесі α-окислення беруть участь пероксид водню і ферменти пероксидаза та альдегіддегідрогеназа жирних кислот:

Альдегід жирної кислоти, що утворився, за участю НАД-залежної дегідрогенази окислюється до жирної кислоти, яка має на один атом вуглецю менше, ніж вихідна кислота:

Далі процес повторюється. Отже, α-окислення жирних кислот є двостадійним процесом.
Біосинтез гліцерину.
В організмах людини і тварин основним шляхом утворення гліцерину є відновлення діоксіацетонмонофосфату – проміжного продукту обміну вуглеводів за участю ферменту гліцерофосфатдегідрогенази:
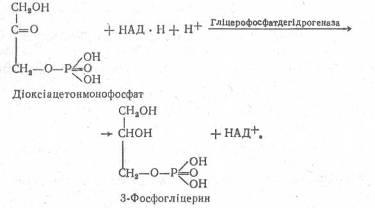
З-Фосфогліцерин, що утворюється внаслідок цієї реакції, є активною формою гліцерину і може використовуватися для синтезу тригліцеридів і фосфоліпідів.
Частина гліцерофосфату при каталітичній дії фосфатази може гідролізуватися з утворенням гліцерину і фосфорної кислоти:
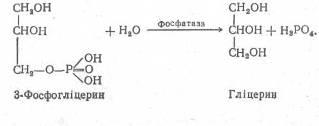
Утворення гліцерину в організмі проходить також при гідролітичному розщепленні тригліцеридів і фосфогліцеридів під впливом тканинних ліпаз.
Біосинтез жирних кислот.
Цей процес, на відміну від β-окислення, проходить у розчинній частині цитоплазми за складним механізмом, який забезпечується рядом факторів і цитоплазматичних ферментних систем. Мітохондрії й ендоплазматичний ретикулум не беруть безпосередньої участі в цьому синтезі. Проте в них здійснюються процеси нарощування (подовження) вуглецевих ланцюгів жирних кислот, які містять від 12 до 16 атомів вуглецю.
Дослідженнями було встановлено, що в процесі синтезу жирних кислот важливу роль відіграють ацетил-КоА, малоніл-КоА, НАДФ.
Н + Н+
, іони гідрокарбонату натрію та двовалентних металів (Mg2+
), а також складний поліферментний комплекс синтетаза жирних кислот.
При дослідженні взаємозв'язку між процесами синтезу і β-окислення жирних кислот було встановлено, що ці два процеси здійснюються за різними механізмами і в різних субцелюлярних структурах. Порівняно з β-окисленням біосинтез жирних кислот має ряд особливостей, які полягають насамперед у тому, що β-окислення жирних кислот проходить у мітохондріях, а синтез – у розчинній фракції цитоплазми. Разом з цим в усіх стадіях синтезу жирних кислот бере участь АПБ–SH, а при β-окисленні жирних кислот – КоА–SH.
Біосинтез тригліцеридів.
Процес проходить у різних органах і тканинах організму при наявності двох вихідних сполук – активного гліцерину (α-фосфогліцерину) та активних жирних кислот (ацил-КоА) і відповідних ферментних систем. Залежно від типу тканин організму біосинтез тригліцеридів може проходити двома шляхами – фосфатидним і β-моногліцеридним.
Перший шлях характерний для більшості органів і тканин організмів людини і тварин. Він розпочинається з ацилюванням вільних гідроксильних груп α-гліцерофосфату двома молекулами ацил-КоА, внаслідок чого утворюється фосфатидна кислота. Реакцію каталізує фермент гліцерофосфатацилтрансфераза:
У цій реакції здебільшого беруть участь насичені і ненасичені С16
–С18
похідні КоА.
У клітинах фосфатидна кислота міститься в мізерних кількостях. Однак, незважаючи на це, вона є важливою проміжною сполукою, що утворюється при синтезі як тригліцеридів, так і фосфоліпідів.

На наступній стадії біосинтезу тригліцеридів фосфатидна кислота, що утворилась, піддається гідролізу за участю ферменту α-фосфатид-фосфогідролази. При цьому утворюється α,
β-дигліцерид і виділяється фосфорна кислота:
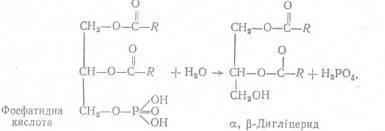
Далі α, β-дигліцерид взаємодіє з іншою молекулою ацил-КоА з утворенням тригліцериду:

Описаний вище процес біосинтезу тригліцеридів називають фосфатидним,
оскільки проміжним продуктом є фосфатидна кислота.
Другий шлях біосинтезу тригліцеридів – моногліцеридний
– характерний в основному для слизової оболонки кишок. Він здійснюється шляхом взаємодії β-моногліцериду з двома молекулами ацил-КоА. При цьому утворюється відповідний тригліцерид. Реакцію каталізує фермент дигліцерид-трансацилаза:
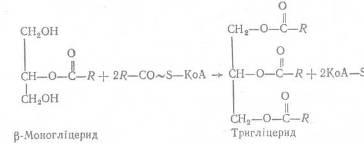 [2, с. 468–487] [2, с. 468–487]
Обмін білків займає центральне місце у всьому різноманітті обмінних процесів організму. Це пояснюється, з одного боку, тим, що всі структурні елементи клітин, тканин і органів людини і вищих тварин побудовані з білків; з іншого боку, маючи специфічні фізико-хімічні і біологічні властивості, білки є тим інструментом, який реалізує геном клітини. Організм людини і тварин не може існувати без регулярного надходження білків із їжею. Якщо на тривалий час вилучити з їжі жири і вуглеводи, то це не викличе в організмі таких тяжких розладів, як відсутність білка. Тривале безбілкове харчування, навіть за інтенсивного вживання з їжею вуглеводів і жирів, неминуче закінчується смертю. Дуже значною є роль білків як пластичного матеріалу. З моменту народження організму і до його смерті постійно відбувається руйнування і відновлення клітин. Пластична функція білків настільки важлива, що ніякими іншими органічними сполуками їх замінити неможливо. Все це потребує обов'язкового надходження в організм білків. У цьому відношенні продукти рослинного походження, що є основним джерелом вуглеводів, мають другорядне значення. Перше місце в забезпеченні організму людини білками займають продукти тваринного походження.
Білки не можуть бути використані організмом у тому вигляді, в якому вони надходять з їжею, оскільки їм властива строго видова специфічність. Більш того, кожний орган і кожна тканина організму людини складаються з характерних для них білків. Якщо ввести, наприклад, у кров людини альбуміни і глобуліни крові якоїсь тварини, то вони будуть поводитись як чужорідні тіла. Тому перед тим, як використовувати білки, що надходять із їжею, організм має позбавити їх видової специфічності. Отже, білки розщеплюються на окремі амінокислоти. Це необхідно ще й тому, що молекули білків не можуть проникати через клітинну мембрану, тоді як амінокислоти вільно через неї проходять. Розщеплення білків на амінокислоти відбувається в травному каналі. Весь же процес обміну білків включає перетравлювання, усмоктування продуктів розщеплення і внутрішньоклітинний обмін.
У слині немає ферментів, що розщеплюють білки. Перетравлювання білків відбувається в шлунку і тонких кишках. Під дією хлороводневої кислоти, що міститься в шлунковому соку, який виділяється слизовою оболонкою шлунку (близько 2,5 л на добу), відбувається набрякання білків, що полегшує їх гідролітичне розщеплення ферментами.
Найбільш важливими ферментами шлункового соку є пепсин і гастриксин. Під дією пепсину відбувається розщеплення пептидних зв'язків у молекулах білків, утворених аміногрупами ароматичних і моноамінодикарбонових амінокислот.
Під впливом цих двох протеолітичних ферментів молекули білків розщеплюються на окремі амінокислоти і поліпептиди різного розміру. У шлунку добре перетравлюються альбуміни і глобуліни як тваринного, так і рослинного походження, погано розщеплюються білки сполучної тканини (колаген і еластин) і зовсім не перетравлюються кератин і протаміни.
Вільні амінокислоти, що утворилися в шлунку, поліпептиди і нерозщеплені білки надходять у дванадцятипалу і тонкі кишки, де зазнають впливу великої групи протеолітичних ферментів, що виробляються підшлунковою залозою і слизовою оболонкою тонкої кишки. Ферменти підшлункової залози надходять у дванадцятипалу і далі в тонку кишку, де змішуються з кишковим вмістом. До складу цієї суміші входять ферменти, які здійснюють розщеплення білків і окремих поліпептидів до вільних амінокислот – трипсину, хімотрипсину, карбоксипептидази, еластази і великої групи три- і дипептидаз. Оптимум дії зазначених ферментів лежить у слаболужному середовищі (рН – 7,8–8,1). Ці ферменти виділяються в просвіт тонкої кишки в неактивному стані у вигляді трипсиногену, хімотрипсиногену, прокарбоксипептидази і проеластази, що перетворюються в активну форму під час надходження в кишки окремих поліпептидів і білків, які не розщепилися.
Під дією ентерокінази
(що виділяється стінкою кишок) або самого трипсину трипсиноген
перетворюється в активний трипсин, який виявляє максимальну активність при рН – 7,0. Він розщеплює пептидні зв'язки, утворені карбоксильними групами аргініну і лізину, у будь-якому місці поліпептидного ланцюга.
Активний хімотрипсин
гідролізує пептидні зв'язки, утворені карбоксильними групами триптофану, фенілаланіну або тирозину, а також лейцину і метіоніну.
Кінцеві пептидні зв'язки розщеплюють карбоксипептидази.
Відомі карбоксипептидази А і В. Перша розщеплює всі СООН-кінцеві пептидні зв'язки за винятком тих, де знаходяться СООН-залишки лізину або аргініну. Друга, навпаки, гідролізує тільки ті кінцеві пептидні зв'язки, що утворені СООН-групами лізину й аргініну.
Еластаза
розщеплює пептидні зв'язки між залишками різних нейтральних кислот. Слизова оболонка тонкої кишки секретує амінопептидазу під назвою лейцинамінопептидаза.
Цей фермент, незважаючи на свою назву, має слабо виражену специфічність і відщеплює NH2
-кінцеві залишки більшості амінокислот.
Так, у результаті спільної дії різних протеолітичних ферментів, що виділяються стінкою шлунка, підшлунковою залозою і стінкою тонкої кишки, харчові білки зазнають повного гідролітичного розщеплення до вільних амінокислот. Останні всмоктуються клітинами стінки тонкої кишки, звідки потім надходять у кров і розносяться по всіх органах і тканинах, де відбувається подальше перетворення.
У клітинах окремих органів і тканин амінокислоти зазнають різних перетворень. Утворенню кінцевих продуктів білкового обміну передує попереднє внутрішньоклітинне окиснення амінокислот. При цьому для окиснення двадцяти різних амінокислот, що входять до складу білків, існує і двадцять різних шляхів, кожний з яких: свою чергу складається з великої кількості ферментативних ре акцій. Шляхи включення вуглецевих скелеті двадцяти амінокислот у цикл Кребса показані на схемі:
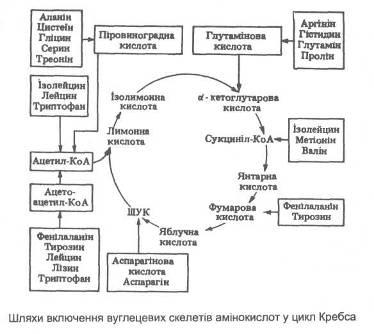
Перетворення амінокислот в організмі, людини відбувається переважно в клітинах печінки, нирках і незначною мірою – у клітинах скелетних м'язів. Перед включенням вуглецевих скелетів вільних амінокислот у цикл Кребса відбувається їх дезамінування.
Дезамінування амінокислот.
Найбільш важливими процесами, за допомогою яких відбувається відщеплення аміногруп від амінокислот у ссавців, є трансамінування й окиснювальне дезамінування.
Трансамінування є складним процесом, що відбувається у два етапи. На першому етапі здійснюється перенос NH2
-групи від амінокислоти на фосфопіридоксаль амінотрансферази. При цьому амінокислота перетворюється у відповідну кетокислоту, а фосфопіридоксаль у фосфопіридоксамін:
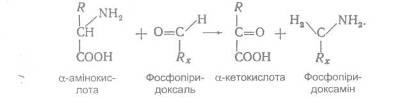
На другому етапі аміногрупа з фосфопіридоксаміну передається на кетокислоту, яка перетворюється в амінокислоту:
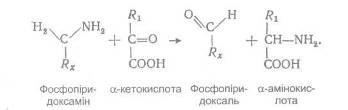
Отже, незалежно від початкових реакцій трансамінування кінцевим акцептором аміногруп більшості амінокислот є а-кетоглутарова кислота. Перетворюючись у глутамінову кислоту, вона служить каналом, за допомогою якого аміногрупи передаються в заключну серію реакцій, які ведуть до утворення кінцевих продуктів азотистого обміну.
Окиснювальне дезамінування
полягає у відщепленні аміногрупи від амінокислот з виділенням аміаку. Аміногрупи різних амінокислот, зібрані в складі глутамінової кислоти, звільняються у вигляді іонів NH4
+
:
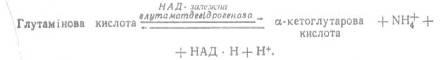
Відомі й інші шляхи дезамінування а-амінокислот, такі, як відновне, гідролітичне і внутрішньомолекулярне:
а) відновне дезамінування:
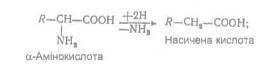
б) гідролітичне дезамінування:
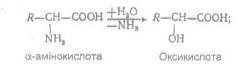
в) внутрішньо молекулярне дезамінування:
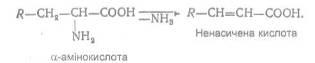
Ці види дезамінування α-амінокислот найбільш характерні для мікроорганізмів і рослин.
Декарбоксилювання амінокислот
є одним із шляхів перетворення амінокислот, утворених в результаті гідролітичного розщеплення білків їжі. У результаті реакцій декарбоксилування амінокислот у тканинах людини і вищих тварин утворюються аміни.
Аміни
(тирамін, адреналін, гістамін, серотонін і ін.) – це біологічно активні речовини, деякі з них є отрутами. Аміни виконують в організмі важливу роль. Так, гістамін, тирамін і серотонін мають потужний фармакологічний вплив на кров'яний тиск і кровоносні судини.
Проте реакції декарбоксилування амінокислот на відміну від реакцій переамінування не є основним шляхом перетворення амінокислот, незважаючи на велике фізіологічне значення утворених продуктів реакції. Швидкість цих реакцій дуже мала.
У результаті різних перетворень амінокислот у тканинах організму утворюються аміак, вуглекислий газ і вода.
Після дезамінування α-амінокислот утворюються безазотисті сполуки. Ми вже знаємо, що в основному це α-кетокислоти, які на певних ділянках включаються в цикл трикарбонових кислот, де піддаються дегідруванню і декарбоксилюванню, і зрештою перетворюються в Н2
О і СО2
.
Деякі кетокислоти, зазнаючи окислювального декарбоксилування, утворюють кислоти з різною хімічною структурою, залежно від якої в одних випадках вони окиснюються шляхом перетворення вуглеводів. Проте й у цих випадках врешті-решт утворюються СО2
і Н2
О. Вуглекислий газ частково виводиться з організму, частина, що залишилася, використовується для синтетичних процесів, наприклад, для синтезу вищих жирних кислот, пуринових основ та ін.
Якість білкового харчування
Білки, як уже відомо, є основним пластичним матеріалом нашого організму, який іншими речовинами замінити неможливо.
Білки відрізняються один від одного вмістом окремих амінокислот. Тому залежно від амінокислотного складу для покриття потреб організму в білку необхідна різна кількість окремих білків. Різні білки мають неоднакову біологічну цінність. Чим ближчий амінокислотний склад того або іншого білка до складу білків даного організму, тим вища його біологічна цінність.
Найбільш цінними є білки, які в достатній кількості містять всі необхідні організмові незамінні амінокислоти (тобто такі, що в організмі зовсім не синтезуються або синтезуються в дуже малій кількості).
Таким чином, біологічна цінність білка визначається якісним і кількісним складом амінокислот, що входять до його молекули.
Для людини цінними є білки молока, м'яса і курячого яйця, із рослинних білків – білок картоплі, що за своєю біологічною цінністю перевищує не тільки білок хліба, але й за деякими амінокислотами навіть білок коров'ячого молока.
Обмін речовин в організмі як один з основних проявів життєдіяльності – єдиний біологічний процес. Всі перетворення речовин і енергії, процеси синтезу і розкладання, анаболізму і катаболізму взаємозв'язані, взаємозумовлені і тонко координовані нейрогуморальними механізмами, що забезпечує існування організму як єдиної впорядкованої високоорганізованої системи.
Обмін основних класів органічних сполук – білків, вуглеводів і ліпідів – є єдиним метаболічним процесом, який підлягає основним діалектичним закономірностям взаємозалежності, взаємоузгодженості і взаємоперетворення. Тому неможливо уявити в живих системах ізольованого перетворення кожного з цих класів органічних сполук. У клітинах організму перетворення жирів, білків і вуглеводів, їх розщеплення і синтез здійснюються одночасно й узгоджено, внаслідок чого забезпечується сукупність метаболічних реакцій, які становлять гармонічний баланс організму, що нормально функціонує.
З біохімічної точки зору взаємозв'язок між перетворенням вуглеводів, білків і ліпідів виявляється в тому, що з вуглеводів їжі за певних умов можуть утворюватись ліпіди, а з білків – вуглеводи. Тому при нестачі вуглеводів потреба в білках зростає, а недостатнє надходження ліпідів може компенсуватись вуглеводами.
Взаємозв'язок між цими класами органічних сполук можна розглядати в двох аспектах – перетворення вуглеводів на ліпіди (ліпогенез за рахунок вуглеводів) і перетворення ліпідів на вуглеводи.
Синтез жирів із вуглеводів.
Протікання процесу перетворення вуглеводів на ліпіди було доведено численними спостереженнями й експериментальними дослідженнями. У людей, які споживають велику кількість борошняних і кондитерських виробів, часто спостерігається ожиріння. З енергетичної точки зору процес перетворення вуглеводів на жири слід розглядати як депонування енергії, хоч синтез жиру теж супроводжується певними енергетичними затратами, які компенсуються підчас окислення їх до кінцевих продуктів.
З біохімічної точки зору процес перетворення вуглеводів на жири можна досить легко обґрунтувати. Відомо, що молекула жиру побудована з гліцерину і вищих жирних кислот. Отже, основні процеси перетворення вуглеводів у ліпіди зводяться до утворення цих основних компонентів жиру.
Біосинтез вищих жирних кислот, необхідних для синтезу ліпідів, здійснюється за участю центрального метаболіту вуглеводного обміну – піровиноградної кислоти, в результаті окислювального декарбоксилування її і утворення активного ацетату – ацетил-КоА. Ацетил-КоА вступає у реакцію конденсації, внаслідок чого утворюється ацетооцтова кислота, з якої далі синтезуються одноосновні високомолекулярні кетокислоти, які беруть участь в утворенні жирних кислот.
Отже, синтез жирних кислот із вуглеводів здійснюється через ацетил-КоА. Це припущення повністю підтверджено дослідженнями з застосуванням мічених атомів. Так, при введенні в організм оцтової кислоти, міченої атомами радіоактивного вуглецю (14
С), їх було виявлено в ацетооцтовій кислоті і високомолекулярних жирних кислотах – складових компонентах жиру. Активна форма гліцерину і жирні кислоти (у вигляді ацил-КоА) використовуються для синтезу жиру.
Нижче наведено загальну схему перетворення вуглеводів на ліпіди»
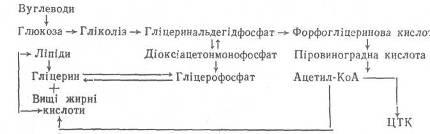
Синтезвуглеводівізліпідів.
Питання про можливість синтезу вуглеводів із ліпідів довгий час було дискусійним, оскільки існувало дві протилежні точки зору. Однак на основі численних досліджень і експериментальних даних було доведено можливість синтезу вуглеводів із ліпідів, хоч цей процес не є обов'язковим для організму і частіше спостерігається за певних фізіологічних умов.
Важливим підтвердженням можливості синтезу вуглеводів із ліпідів послужили дані з вивчення проміжних продуктів обміну вуглеводів та ліпідів в організмах людини і тварин, а також ферментних систем, які каталізують ці реакції. Виявилось, що спільним проміжним продуктом обміну вуглеводів і ліпідів є ацетил-КоА, який утворюється під час β-окислення жирних кислот і окислювального декарбоксилювання піровиноградної кислоти. Саме ацетил-КоА і є сполучною ланкою між обміном вуглеводів і ліпідів і становить молекулярну основу перетворення вуглеводів на ліпіди і ліпідів на вуглеводи.
Однак це не означає, що весь ацетил-КоА, що утворюється під час β-окислення жирних кислот, використовується для синтезу вуглеводів, а утворена при розщепленні вуглеводів ацетооцтова кислота перетворюється на жири.
Крім синтезу вуглеводів з ацетил-КоА незначна кількість їх може утворюватись із гліцерину – продукту розщеплення жирів шляхом окислення його в діоксіацетонмонофосфат і гліцеринальдегідмонофосфат. Разом з цим гліцеринальдегідмонофосфат здатний окислюватись до ацетил-КоА, який використовується для синтезу глікогену.
Між обміном цих класів органічних сполук існує тісний взаємозв'язок, який полягає в можливості їх взаємного перетворення в ході метаболічних процесів. При цьому важливим у біологічному відношенні є перетворення білків на вуглеводи і обмежене значення має перетворення вуглеводів на білки.
Синтез вуглеводів із білків.
Найінтенсивніше вуглеводи синтезуються з тих амінокислот, які в процесі метаболізму перетворюються на піровиноградну кислоту. Такі амінокислоти дістали назву глюкогенних.
Це аспарагінова і глутамінова кислоти, серин і валін, орнітин, цистеїн, гліцин, аланін, метіонін, гістидин та ін. Глюкогенні амінокислоти після переамінування і дезамінування перетворюються на кетокислоти – щавлевооцтову, α-кетоглутарову, піровиноградну. Серед них саме піровиноградна кислота є основним метаболітом, який забезпечує перетворення амінокислот на вуглеводи. Щавлевооцтова й α-кетоглутарова кислоти після декарбоксилювання також перетворюються на піровиноградну кислоту.
Перетворення піровиноградної кислоти у вуглеводи може здійснюватись через ацетил-КоА, який утворюється під час її окислювального декарбоксилювання або внаслідок протилежно напрямлених реакцій гліколізу.
Процес перетворення білків на вуглеводи за звичайних фізіологічних умов протікає незначною мірою, оскільки розщеплення амінокислот направлене переважно в бік утворення кінцевих продуктів.
Синтез білків із вуглеводів.
З вуглеводів можна синтезувати амінокислоти, які входять до складу білків. Відомо, що вуглеводи є основним джерелом, з якого в організмі утворюються піровиноградна, щавлевооцтова та α-кетоглутарова кислоти. Дані кетокислоти внаслідок амінування перетворюються на відповідні амінокислоти: аланін, аспарагінову і глутамінову амінокислоти.
Утворення ліпідів із білків.
Експериментально встановлено, що при значному вмісті білків у харчовому раціоні частина їх перетворюється на жири. Сполучною ланкою у цьому процесі є піровиноградна кислота, яка утворюється під час дезамінування і переамінування аланіну, серину та інших амінокислот.
Піровиноградна кислота внаслідок декарбоксилювання перетворюється на ацетил-КоА, який може використовуватись для синтезу вищих жирних кислот.
Піровиноградна й оцтова кислоти можуть утворюватись з аспарагінової і глутамінової амінокислот після їх дезамінування і декарбоксилювання. Амінокислоти, які в процесі перетворення утворюють метаболіти, можуть використовуватись для синтезу жирів і називаються кетогенними.
Деякі амінокислоти мають однакову здатність до перетворення в жири і вуглеводи, тобто вони є глюкогенними і кетогенними (ізолейцин, лізин, фенілаланін, тирозин).
З продуктів білкового обміну може синтезуватись також гліцерин. Так, аланін легко перетворюється в піровиноградну кислоту, яка під час зворотного гліколізу перетворюється в діоксіацетонмонофосфат – спільний метаболіт вуглеводного і жирового обміну, а далі легко перетворюється на гліцерин.
Утворення білків із ліпідів.
Цей процес в організмах людини і тварин має обмежене значення. Однак частковий синтез замінних амінокислот із жирів може здійснюватись з α-кетокислот – піровиноградної, α-кетоглутарової, щавлевооцтової, тобто з тих амінокислот, які легко піддаються амінуванню і переамінуванню.
Центральне місце в перетворенні ліпідів у білки займає α-кетоглутарова кислота, оскільки вона легко піддається прямому амінуванню за участю аміаку і перетворенню в глутамінову. Оскільки з жирів утворюється незначна кількість кетокислот жири не можуть бути важливим джерелом синтезу білків.
Отже, процеси обміну білків, ліпідів і вуглеводів в організмі взаємозв'язані. [6, с. 419–438]
Окисно-відновні реакції мають величезне значення для підтримування життєдіяльності біологічних систем. Процеси фотосинтезу, дихання, травлення – все це ланцюги окисно-відновних реакцій. Ці реакції відіграють чи не найважливішу роль при утворенні власних полімерних компонентів, забезпечуючи організм структурними складовими та енергією.
Проте живий організм є набагато складнішою системою тому і процеси, що в ньому протікають, характеризуються великою складністю, ступінчістю та участю складних ферментативних комплексів.
Живий організм нерозривно пов’язаний з навколишнім середовищем, з якого він одержує необхідні для життя харчові речовини, воду та кисень. З цих речовин в організмі утворюються складні біоорганічні сполуки, які безпосередньо беруть участь у біохімічних перетвореннях.
Життя людини – це складний багатогранний процес, пов’язаний із постійним розщепленням і відновленням в організмі хімічних сполук, що супроводжується витратами енергії. Все це потребує достатнього надходження в організм необхідних неорганічних та органічних речовин, які людина споживає з їжею. Від кількості і якості їжі, режиму харчування залежить рівень функціонального стану, його здоров’я, ріст і розвиток, а також здатність до високопродуктивної розумової і фізичної діяльності.
1. Березов Т.Т., Коровкин Б.Ф. Биологическая химия. – М.: Медицина, 1983. – 752 с.
2. Боєчко Ф.Ф. Біологічна хімія: Навчальний посібник. – К.: Вища школа, 1995. – 536 с.
3. Ленинджер А. Основы биохимии: В 3-х томах. Пер. с англ. – М.: Мир, 1985.
4. Основы биохимии / Под ред. А.А. Анисимова. – М.: Высш. шк., 1986. – 547 с.
5. Романова Н.В. Загальна та неорганічна хімія: Підручник для студентів вищ. навч. закладів. – Київ;Ірпінь: ВТФ «Перун», 1998. – 480 с.
6. Филиппович Ю.Б. Основы биохимии: Учеб. пос. – М.: Высш.шк., 1985. – 503 с.
7. Явоненко О.Ф., Яковенко Б.В. Біохімія: підручник для студентів спеціальності «Фізична культура» педагогічних університетів. – Суми: ВТД «Університетська книга», 2002. – 380 с.
|