, которые нельзя или нецелесообразно подвергать сепарации по группам способом высокотемпературной переработки
Как видно из изложенного в пятой главе материала значительная часть (по весу) ТБО может и должна перерабатываться способом экологической биотехнологии. Другая фракция ТБО, включая стекло, железо, пластмассы и другие виды ТБО также должны перерабатываться в товарные продукты так, как это было изложено в предыдущих главах, посвященных переработке ТПО для каждого вида сырья. Так в частности стеклобой следует направлять на переплавку. Железо и другие металлы также на переплавку. Пластические массы на повторную переработку. Способ переработки этого вида сырья уже излагался в предыдущих главах. Однако есть некоторые особенности при повторной переработке синтетических полимерных материалов. Особенно это касается переработки синтетических смол и пластических масс, содержащих ароматическое ядро и продуктов, которые при переработке при относительно высокой температуре +100-+800°С могли бы выделять галоиды: хлор и/ или бром. Суть этого заключается в том, что при переработке такого синтетического полимера, а также сложного эфира целлюлозы, полученного в среде мелиленхлорида могут в присутствии даже следов галоидов хлора и брома образовываться галоидированные ДО и ДПВ по упомянутой уже во второй главе схеме и повторенной сейчас, а именно.
Пиролиз и хлорирование (бромирование) природных предшественников (1):

В результате образуется типичный галоидированный ДО и ДПВ - полихлордибензодиоксин (полибромдибензодиоксин) и/ или полихлордибензофуран (полибромдибензофуран).
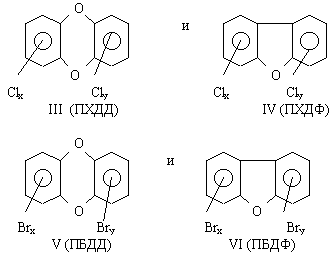
То есть по классификации Л.А. Федорова образуется III, IV, V и VI представитель галоидированных ДО и ДПВ (1). А это страшно и сверхопасно. Кроме того, следует заметить, что в небольших поселках, в небольших городах сепарацию ТБО по видам не целесообразно проводить по технико-экономическим соображениям. Как же поступать с такими видами ТБО, образующихся в сравнительно небольших количествах? Кроме того, как поступать с определенными видами ТПО ряда металлоперерабатывающих производств? Как обходиться, как использовать отработанные химические источники тока (ОХИТ)? И, наконец, куда девать отходы хирургии, стоматологии и т.п.?
Итак, все эти перечисленные виды ТПО и ТБО, а также отходы лечебных учреждений в виду их высокой в первую очередь инфекционной опасности на наш взгляд подлежат высокотемпературной переработке при температуре +1200-+1600°С в течение не менее 4-7 часов производственного цикла для полной стерилизации биологических отходов и полной дегазации супертоксикантов ДО и ДПВ, которые могут существовать в этих видах отходов в качестве побочных продуктов или даже в следах. При таких температурах все компоненты переходят в состояние близкое к плазменному. Для переработки этой категории ТПО и ТБО следует применять технологический процесс "Пурвокс" (2) или электротермический реактор (3), который, как будем надеяться, будет выпускаться в промышленных условиях с разным объемом загрузки и с разной производительностью. На наш взгляд электротермический реактор будет несомненно дешевле при серийном производстве, чем аппарат для проведения технологического процесса "Пурвокс".
6.1. Высокотемпературная переработка ТП и ТБО - гарантия уничтожения всех видов биологических, биохимических продуктов и канцерогенов-супертоксикантов
При загрузке отходов металлоперерабатывающих производств, синтетических полимерных материалов неизвестной химической природы (возможно содержащих в макромолекулярной цепи ароматические кольца, например, полиэтилентерефталата и галоидированных полиолефинов, например, поливинилхлорида), отработанных химических источников тока (ОХИТ), остатков смазочно-охлаждающей жидкости (сож) после металлообработки, хирургических, стоматологических и других биологических отходов лечебных и научно-исследовательских организаций и учреждений и не сепарированных ТБО постепенно в течение нескольких часов необратимо происходит разрушение галоидированных ДО и ДПВ по схеме:
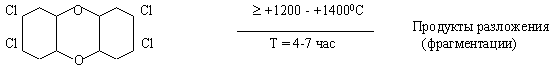
Наиболее опасные компоненты ОХИТ также разлагаются и протекает ряд процессов (4):
Zn+2NH4
Cl+2MnO2
=Zn(NH3
)2Cl+H2
O+Mn2
O3
.....(I)
Zn+2NH4
Cl+1/2O2
=Zn(NH3
)2
Cl2
+H2
O......(II)
Zn+NaOH+1/2O2
=NaHZnO2
......(III)
Zn+CuO+NaOH=Zn(ONa)2
+Cu+H2
O......(IV)
HgO+Zn+2KOH=Hg+K2
ZnO2
+H2
O......(V)
PbO2
+H2
SO4
+Zn=PbSO4
+ZnSO4
+2H2
O.......(VI)
PbO2
+2H2
SO4
+Cd=PbSO4
+CdSO4
+2H2
O......(VII)
PbO2
+4HClO4
+Pb=2Pb(ClO4
)2
+2H2
O......(VIII)
Ag2
O+4KOH+Zn=2Ag+K2
ZnO2
+H2
O......(IX)
Cu2
Cl2
+Mg=2Cu+МgCl2
......(X)
2AgCl+Mg=2Mg+MgCl2
.....(XI)
6Mg+8H2
O+C6
H4
(NO2
)2
=C6
H4
(NH2
)2
+6Mg(OH)2
.....(XII)
Mg+H2
O+2MnO2
=Mn2
O3
+Mg(OH)2
......(XIII)
Итак, в начале процесса термообработки все эти компоненты, приведенные в уравнениях (I) - (XIII) постепенно переходят по мере нагревания массы в жидкое и далее в состояние, близкое к плазменному. В электротермическом генераторе (ЭТГ), где количественно преобладает углерод (С) в виде графита и чугун в виде элементарного Fe (при больших загрузках ТПО металлоперерабатывающих производств) до его окислов FeO, Fe2
O, вода поступающая в реактор переходит в парообразное состояние. Протекают процессы:
H2
O+C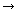 H2
+CO.........(XIV)...........(5) H2
+CO.........(XIV)...........(5)
То есть образуется водяной газ. При наличии паров воды, кроме того происходит процесс:
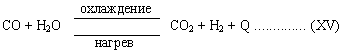
При этом следует заметить, что в верхней части реактора, где температура ниже преобладает процесс 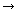 с образованием CO2
и H2
. В нижней части реактора, где преобладает более высокая температура преобладают процессы и образуются продукты СО+Н2
О. При этом СО оксид углерода образуется при очень высоких температурах, когда диоксид углерода СО2
неустойчив (6). Процесс образования водяного газа эндотермичен, поэтому углерод охлаждается. Однако, поскольку в реакторе температура t>+1000°С происходит процесс (6): с образованием CO2
и H2
. В нижней части реактора, где преобладает более высокая температура преобладают процессы и образуются продукты СО+Н2
О. При этом СО оксид углерода образуется при очень высоких температурах, когда диоксид углерода СО2
неустойчив (6). Процесс образования водяного газа эндотермичен, поэтому углерод охлаждается. Однако, поскольку в реакторе температура t>+1000°С происходит процесс (6):

Процессы (XVI) и (XVIа) протекают при взаимодействии воздуха с раскаленным углеродом. В результате получается смесь СО+N2
, т.е. образуется генераторный газ. В итоге в отходящих газах из реактора содержится водяной газ: СО+Н2
и генераторный газ СО+N2
. Синтез аммиака из газообразных N2
и Н2
не происходит, т.к. этот процесс может происходить при низких температурах и при высоком давлении (7). При высоких температурах происходит разложение ОХИТ:
Q+NH4
Cl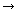 NH3
+HCl...........(XVII) (7) NH3
+HCl...........(XVII) (7)
Разложение Zn (NH3
)2
Cl2
происходит при его плавлении при нагревании по схеме:
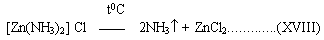
Аналогично разрушается комплекс:
[Hg(NH3
)2
]Cl2
..................
ZnCl2
в таких условиях выкипает (8). Однако по мере выхода из реактора ZnCl2
оседает (конденсируется) на сравнительно холодных поверхностях трубопроводов.
Синтез синильной кислоты HCN сильнейшего яда в данных условиях маловероятен, т.к. он происходит хотя и при нагревании до температуры t>+500-+600°С, но в присутствии особых катализаторов (диоксида церия СеО2
(6) или в присутствии диоксида тория ThO2
(7)):
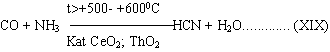
Ни того, ни другого катализатора у нас в системе нет. Кроме того, рабочая температура процесса значительно больше +500-+600°С.
Кроме того, возможно протекание следующих процессов:
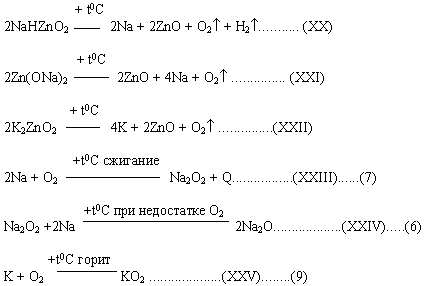
ZnO при +1950° возгоняется при более высокой температуре, разлагается до Zn и O2
(8):
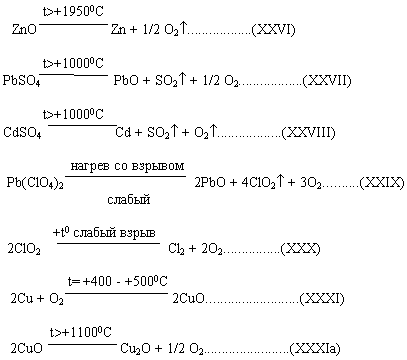
Хлористый магний MgCl2
сначала плавится при t=+718°С, затем при t=+1412°С кипит.
"Кальцинированная" сода, входящая в состав сож разлагается:
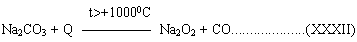
При высокотемпературной обработке ТБО образуются следующие вещества:
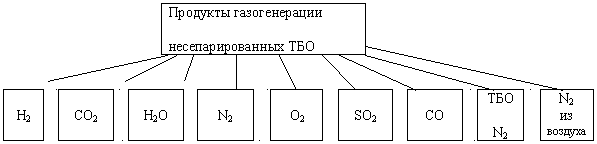
Вполне естественно из не сепарированных ТБО токсичных веществ не образуется, если не считать SO2
, который может образоваться из ТБО (за счет термического разложения меркантанов). Из СОЖ продуктами газогенерации могут быть:
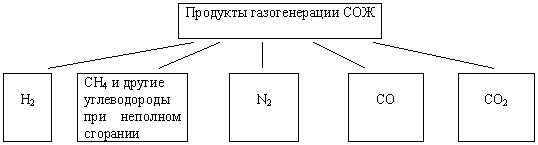
Таким образом при высокотемпературной переработке не сепарированных ТБО, остатков СОЖ продуктами газогенерации являются следующие компоненты:
- Так называемый генераторный газ: CO+N2
;
- Так называемый водяной газ: СО+Н2
.
В процессе электротермического воздействия на ОХИТ происходит также разложение фенилендиамина C6H4(NH2) до CO; CO2
; N2
и H2
. В кубовых остатках, в шлаке остается большой комплекс веществ, а именно:
Железо и небольшое количество окислов его. Эти вещества составляют (в зависимости от соотношения загружаемых компонентов) значительную часть, возможно до 70-90% от общей массы шлака. В шлаке также должно содержаться небольшое количество MgSiO3
и CaSiO3
из ТБО, CuO и Cu2
O; PbO; очень немного ZnCl2
; Cd (почти в следах); MgO; Mn3
O4
(Mn3
O4
синтезируется по реакции:
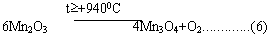
Кроме того в шлаке могут содержаться MgCl2
(частично выкипает при t=+1412°С) в следах NaOH; KOH; в следах Ag и AgCl (AgCl кипит при t=+1550°С)(8) и Hg.
Продукты, которые образуются при разложении ОХИТ следующие:
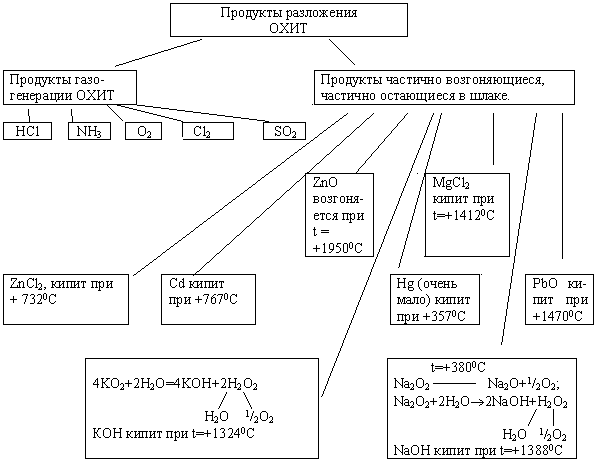
Все возгоняющиеся продукты практически осаждаются на трубах в процессе охлаждения выделяющейся массы газагенератов и возгоняющихся веществ не доходят до барботеров-поглотителей. Таким образом, в тоже время при электротермической обработке всех ранее упомянутых отходов (отходов металло-перерабатывающих производств, несепари-рованных ТБО, ОХИТ, остатков СОЖ и биообъектов) между газообразными продуктами могут происходить следующие процессы:
SO2
+ Cl2
= SO2
Cl2
..................(XXXIII).......(6)
SO2
Cl2
+ 2H2
O = H2
SO4
+ 2HCl..............(XXXIIIa)..........(6)
нагрев
Cl2
+ H2
O + Q = HCl + HClO...........(XXXIV).......(7)
HCl + aq = HCl. aq + Q.................(XXXIVa)........(7)
CO + Cl2
= COCl2
.....................(XXXV)..............(6) (7)
Таким образом возможно образование оксохлорида углерода или фосгена. Под воздействием паров воды фосген медленно гидролизуется:
COCl2
+ 2H2
O ---- 2HCl + H2
CO3
.................(XXXVa)........(6) (7)
Самыми нежелательными процессами являются следующие:
- Образование хлора;
- Образование хлористого сульфурила;
- Образование оксохлорида углерода (фосгена).
Как подавить эти процессы? Самое реальное в наших условиях обильное орошение синтез-газа водой или даже барботирование синтез-газа через слой воды в барботерах так, чтобы в максимальной степени протекали процессы поглощения вредных газообразных веществ водой, а именно процессы (XXXIIIa), (XXXIV), (XXXIVa), (XXXVa). Тем не менее, чтобы полностью обезопасить течение процесса и исключить выброс в отходящих газах Cl2
; SO2
Cl2
; COCl2
следует предусмотреть вторую и третью степень барботирования синтез-газа водой для полного поглощения вредных газов и протекания вышеупомянутых процессов на 100%. Кроме того, предлагается при вышеупомянутой загрузке отходов производить минимальную загрузку ОХИТ, которые являются самыми экологически опасными компонентами - генераторами хлора со всеми вытекающими последствиями в том числе и с возможностью образования галоидированных ДО и ДПВ.
Для разделения разбавленных кислот предлагаются следующие приемы:
После проведения каждой технологической операции производить анализ жидкости из соответствующих емкостей на наличие:
а) серной кислоты, H2SO4 на первых порах качественно введением водного раствора BaCl2 и наблюдением выпадения белого творожистого осадка BaSO4 по реакции: H2
SO4
+BaCl2
=BaSO4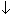 +2HCl............(XXXVI)
+2HCl............(XXXVI)
и количественно по наличию сульфат-иона SO4
--
;
б) соляной кислоты HCl сначала качественно введением водного раствора AgNO3
и выпадением белого осадка AgCl по реакции:
HCl+AgNO3
=AgCl+HNO3
.................(XXXVII)
а затем количественно по наличию хлор иона;
в) угольной кислоты H2
CO3
качественно введением BaCl2
или введением Ca(OH)2
и образованием осадков по реакциям:
BaCl2
+H2
CO3
=BaCO3 +2HCl..................(XXXVIII)
+2HCl..................(XXXVIII)
H2
CO3
+Ca(OH)2
=CaCO3 +H2
O
+H2
O
и количественно по наличию карбоний0иона.
В принципе возможны накладки всех процессов друг на друга. Это конечно может осложнить разделение кислот. Во всяком случае при введении BaCl2
могут происходить оба процесса (XXXVI) и (XXXVIII), т.е. могут осаждаться BaSO4
и BaCO3
. Таким образом, применяя одни и те же реагенты можно жидкость из соответствующих емкостей (из поглотителей) подачей водного раствора BaCl2
перевести в технически слабый водный раствор соляной кислоты HCl.
Итак, рассмотрим один из прогнозируемых вариантов технологии переработки ТП и БО в электротермическом реакторе (ЭТР).
6.2. Прогнозируемая технология переработки ТП и БО в электротермическом реакторе (ЭТР) (один из возможных вариантов)
Для соблюдения правил техники безопасности конструктивно предусматривается наличие предохранительного клапана для возможного сброса максимального давления в I и II камерах ЭТР.
Для переработки ТП и БО в ЭТР, как уже упоминалось используются следующие виды отходов:
- ТО лечебных и научно-исследовательских организаций и учреждений (включая использованные бинты, тампоны, отходы хирургии и стоматологии и т.п.), т.е. ТО, содержащие остатки различных a-аминокислот:
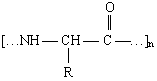 где R - CH3
; C2
H5
; CH2
C6
H5
и т.д. и [С6
H7
O2
(OH)3
]n где R - CH3
; C2
H5
; CH2
C6
H5
и т.д. и [С6
H7
O2
(OH)3
]n
- Синтетические высоко-, олиго- и низкомолекулярные органические вещества, содержащие хлор или бром (в том числе галоидированные полиолефины), а также природные высокомолекулярные полимеры (в том числе целлюлозосодержащие материалы, подвергнутые в процессе облагораживания отбелке хлорсодержащими компонентами):
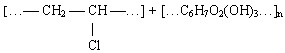
- Отработанные химические источники тока (ОХИТ) - смесь различных неорганических и некоторых органических (C6
H4
(NH2
)2
и (C6
H4
(NO2
)2
) веществ в том числе хлорсодержащих;
- Смазочные охлаждающие жидкости (СОЖ) с отходами черных и цветных металлов.
При переработке ОХИТ они загружаются, как уже упоминалось, в минимальных количествах в ЭТР.
Для переработки ТП и БО предусматриваются следующие температурные режимы в камерах ЭТР:
I камера
В нижней зоне t > +1200 - +1600°С
В средней зоне tmax
>+1200 - +1400°C
В верхней зоне tmax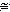 +500 - +800°С
+500 - +800°С
II камера
В нижней зоне t > +1200 - +1400°С
В средней зоне t 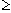 +1000 - +1200°C +1000 - +1200°C
В верхней зоне t 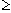 +300 - +400°C +300 - +400°C
Описание технологического процесса
В зависимости от объема электротермического реактора (ЭТР) в него загружаются в соответствующих количествах ТП и БО, производится постепенный разогрев камер и в соответствии с временным технологическим регламентом подается вода. Начинается течение технологического процесса в соответствии с регламентом. По мере протекания технологического процесса в соответствии с одним из прогнозируемых вариантов химико-технологического процесса начинается процесс газовыделения и образования одного из основных продуктов газогенерации - синтез-газа. Одновременно в соответствии с регламентом предусматривается абсорбция вредных и очень токсичных примесей в тарельчатых колоннах со сливными устройствами, изображенных на рис. 14.
Рис. 14. Тарельчатая колонна со сливными устройствами для поглощения вредных газов (в разрезе): 1 - тарелка; 2 - сливное устройство.
По мере абсорбции в тарельчатых колоннах (см. рис. 14 и рис. 15) поз. 1,2,3 (см. рис. 15) образуется смесь слабых минеральных кислот (H2
SO4
; HCl; H2
CO3
), которые в соответствии с регламентом подаются в накопительные сборники поз. 4,5,6. Далее, по мере заполнения накопителей, смесь кислот подается в аппарат поз.7 (рис. 15), куда в
Рис. 15. Технологическая схема работы электротермического реактора ЭТР с установкой по улавливанию токсичных выбросов (один из прогнозируемых вариантов).
соответствии с регламентом периодически подается слабый раствор BaCl2
и происходит выпадение осадков:
BaCl2
+H2
SO4
=BaSO4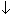 +2HCl
+2HCl
BaCl2
+H2
CO3
=BaCO3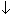 +2HCl
+2HCl
Аппарат (поз. 7) представляет из себя вертикальный реактор с якорной мешалкой Изготовлен из обычной стали и покрытый изнутри стеклоэмалью.
Таким образом в жидкой фазе остается водный раствор слабой соляной кислоты HCl. В осадок выпадает смешанная соль BaSO4
·BaCO3
. Далее суспензия BaSO4 Ч BaCO3 с остатками HCl направляется на центрифугирование в центрифугу (поз.8), где остатки HCl отделяются от осадка и направляются в емкость (поз.7) или прямо в специальную емкость сборник HCl (поз.11). Смесь солей после промывки водой и дробления пневмотранспортом направляются в емкость (поз.9), где производится нагрев этой смешанной соли. При этом сульфат бария BaSO4
плавится при t=+1580°С, а витерит разлагается:
BaCO3
+ Q 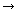 BaO+CO2 BaO+CO2
Далее смесь BaSO4
·BaO охлаждается и после дробления направляется в емкость (поз.10). Емкость (поз.10) представляет из себя вертикальный аппарат с якорной мешалкой. Туда же подается вода для растворения ВаО и образования баритовой воды:
BaO+H2
O=Ba(OH)2
+Q............(7)
Баритовая вода остающаяся в растворе после перемешивания по регламенту идет в сборник, как товарный продукт. Сульфат бария BaSO4
в виде водной суспензии направляется на фугование (на рис. 15 не указано) и на сушку. При получении BaSO4
для медицинских целей продукт направляется сначала на перемывку, затем на фугование и уже потом на сушку.
Завершение процесса контролируется визуально по окончании пробулькивания газа в колоннах (поз.1,2,3) и инструментальными способами (соответствующими КИП). Разумеется предлагаемая прогнозируемая схема разделения кислот в процессе опытных испытаний потребует корректировки и уточнения. Так в частности вопрос о выборе емкости (поз.9) является весьма приближенным и потребуется существенная корректировка этой операции и главное существенная корректировка выбора аппарата (поз.9).
После завершения химико-технологического процесса переработки ТП и БО из ЭТР выгружается шлак, представляющий собой твердый многокомпонентный раствор. Шлак может быть различным в зависимости от загружаемых ТП и БО. Если загружается значительная часть СОЖ с отходами металла, то такой шлак может содержать металл до 70% и более. Такой шлак целесообразно использовать в зависимости от химического состава для переплавки скажем в чугун. Если СОЖ с остатками металла составляет незначительный процент от общего количества загружаемых ТП и БО, то можно прогнозировать, что конечный твердый продукт шлак будет мало содержать металла. Такой шлак нужно направлять на дробление и использовать его в качестве наполнителя для получения цементных растворов. Для этого в цементный раствор, находящийся в двухшнековом смесителе Вернера-Пфлейдерера разгружается дробленый шлак. После окончания загрузки шлака в заданном количестве производится перемешивание цементного раствора до полной гомогенности (однородности). После получения однородной массы производится формование строительных изделий (блоков и т.п.). Использовать шлак для дорожного строительства нельзя, т.к. при переработке ОХИТ возможно образование количественно кадмия (Cd) в шлаке после переработки в ЭТР. А кадмий, как известно, является опасным мутантом и в процессе эксплуатации дорожного покрытия он может медленно при старении покрытия экстрагироваться в близлежащий почвенный слой, что недопустимо.
Таким образом, в процессе переработки ТП и БО получаются следующие товарные продукты:
1. Синтез-газ или точнее смешанный газ представляющий смесь генераторного газа СО+N2
и водяного газа СО+Н2
. Смешанный газ является хорошим энергоносителем. При сжигании 1м3
такого газа образуется ~2800-5000 ккал;
Шлак - твердый продукт, который следует использовать по двум направлениям:
а) при высоком содержании металла такой шлак следует направлять на переплавку; после обогащения и очистки для получения чугуна;
б) при низком содержании металла шлак используется как наполнитель для приготовления цементных растворов и последующего формования строительных блоков и т.п.;
- Слабая (разбавленная) техническая соляная кислота (HCl);
- Сульфат бария - технический продукт, или, если он подвергается очистке, то его уже можно использовать в качестве медицинского препарата (для анализа секреторной деятельности желудка человека);
- Баритовая вода - Ba(OH)2
используется как химический реагент при проведении химического анализа газов на содержание CO2
; SO3
и т.д.
Для выброса в окружающую природную среду вредных газообразных, жидких и твердых продуктов при данной переработке ТП и БО в электротермическом реакторе просто не образуется, если не считать диоксида углерода, образующегося при разложении BaCO3
. Все получающиеся и перечисленные выше продукты жидкие, твердые и газообразные являются товарными продуктами. При сжигании синтез-газа не образуются никакие токсичные вещества.
Литература
-
Л.А. Федоров, Диоксины, как экологическая опасность: ретроспектива и перспективы, М., Наука, 1993, с.1-226.
-
В.Н. Сариев, Пути достижения оптимального хозяйствования твердыми муниципальными отходами//Информ. Сборник "Экология городов", М., №5, 1995, с.73-75.
-
А.Н. Сачков, К.С. Никольский, Ю.И. Маринин, О высокотемпературной переработке твердых отходов во Владимире//Информ. Сборник "Экология городов", М., №8, 1996, с.79-81.
-
Краткая химическая энциклопедия, М., С.Э., т.5, 1967, с.644-653.
-
Прокофьев В.И., Харитонова Н.Д., Митрофанова Н.М., Очистка стоков цеха переработки химических продуктов, Ж.//Кокс и химия, №11, 1985, с.51-53.
-
М.Х. Карапетьянц, С.И. Дракин, Общая и неорганическая химия, М., Химия, 1981, с.358-361, с.598, с.364-365, с.302, с.454, с.319, с.601, с.482, с.585, с.547.
-
Б.В. Некрасов, Курс общей химии, М., ГХИ, 1962, с.338-340, с.237, с.426-427, с.634-643, с.670-643, с.670-672, с.683.
-
Краткий справочник химика, Под ред. В.И. Перельмана, М., ГХИ., 1963, с.96-97, с.90-91, с.68-69, с.80-81, с.62-63, с.78-79.
-
Н.С. Ахметьев, Общая и неорганическая химия, М., ВШ, 1981, с.492.
|