|  3 Расчёт тарельчатого абсорбера 3 Расчёт тарельчатого абсорбера
3.1 Определение условий равновесия процесса
Определим равновесные концентрации ацетона в воде. В случае абсорбции хорошо поглощаемых газов (паров) расчет равновесных концентраций ведут по закону Рауля [2] c.16:
 , (3.1) , (3.1)
где Õ ‑ давление в абсорбере, Па;
Pн
‑ давление насыщенных паров ацетона при температуре абсорбции (t=26 °C), Па;
x*
‑ равновесная концентрация ацетона в воде,  ; ;
у ‑ концентрация ацетона в воздухе,  . .
Давление насыщенных паров ацетона при температуре абсорбции (t = 26°С) по [3] рисунок XIV равно 244 мм. рт. ст. Пересчитаем в Па:
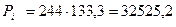 Па Па
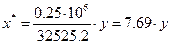 , (3.2) , (3.2)
Величины равновесных концентраций в жидкости достаточно рассчитать для диапазона значений концентраций в газовой фазе от нуля до величины, которая в 1,2-1,5 раз превышает начальную концентрацию абсорбтива.
Для упрощения расчетов материального баланса необходимо сделать пересчет абсолютных концентраций в относительные. Связь между относительной концентрацией и абсолютной выражается следующей формулой по [3] c.283:
 , (3.3) , (3.3)
 , (3.4) , (3.4)
где у ‑ абсолютная концентрация ацетона в газовой фазе,  ; ;
Y ‑ относительная концентрация ацетона в газовой фазе,  ; ;
x ‑ абсолютная концентрация ацетона в жидкой фазе,  ; ;
X ‑ относительная концентрация ацетона в жидкой фазе,  ; ;
Таблица 3.1 - Расчет равновесной линии
| x*,
|
y, 
|
X*, 
|
Y, 
|
| 0
|
0
|
0
|
0
|
| 0,077
|
0,01
|
0,083
|
0,01
|
| 0,15
|
0,02
|
0,18
|
0,02
|
| 0,23
|
0,03
|
0,30
|
0,03
|
| 0,31
|
0,04
|
0,45
|
0,042
|
| 0,38
|
0,05
|
0,61
|
0,053
|
По определенным значениям концентраций строится линия равновесия Х* = m∙Y (рисунок 3.1).
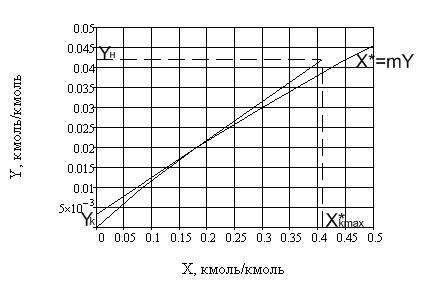
Рисунок 3.1 – Линия равновесия. Определение минимального расхода поглотителя
Коэффициент распределения m найдем как тангенс угла наклона линии равновесия к оси Х. Поскольку линия равновесия в данном случае не прямая, то коэффициент распределения будем рассчитывать как среднее арифметическое, разбив линию равновесия на ступени и рассчитав тангенс угла наклона на каждой из них. Проделав эти операции, получили, что коэффициент распределения m равен 0,1006 кмоль воды/кмоль воздуха.
3.2
Расчет материального баланса
3.2.1 Определение молярного расхода компонентов газовой смеси
Пересчитаем объемный расход при нормальных условиях (T0
=273K, P0
=1,013×105
Па) в объемный расход при условиях абсорбции (Т=299К, Р=0,25×106
Па).
 , (3.5) , (3.5)
где Vсм0
– расход при нормальных условиях, 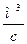 . .
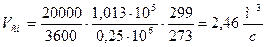 . .
Для удобства дальнейших расчетов переведем объемный расход газовой смеси в молярный.
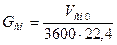 , (3.6) , (3.6)
где Vсм0
‑ объемный расход газовой смеси при нормальных условиях,  ; ;
Gсм
‑ молярный расход газовой смеси,  . .
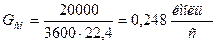 . .
Молярный расход инертного газа определяется по уравнению [2] c.17:
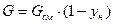 , (3.7) , (3.7)
где ун
‑ исходная концентрация ацетона в газовой смеси,  ; ;
G ‑ молярный расход инертного газа,  . .
Из условия задания ун
=0,04 . .
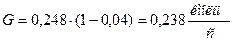 . .
Концентрацию ацетона на выходе из абсорбера yк
,  находим по формуле [2] c.17: находим по формуле [2] c.17:
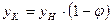 , (3.8) , (3.8)
где j – степень извлечения, j=0,92 (из задания).
 . .
Величины yк
, yн
пересчитаем в относительные по формуле (3.3):
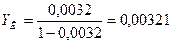
 , ,
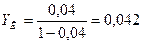  . .
Для определения молярного расхода ацетона M
, который поглощается, служит следующее уравнение [2]:
 , (3.9) , (3.9)
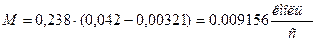 .
.
Для определения минимального молярного расхода чистого поглотителя Lмин
служит следующее уравнение [2]:
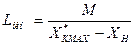 , (3.10) , (3.10)
где X*к
‑ равновесная относительная концентрация ацетона в воде на выходе из аппарата,  ; ;
Хн
‑ исходная относительная концентрация ацетона в воде,  . .
Равновесную относительную концентрацию ацетона в воде на выходе из аппарата определим по линии равновесия (рисунок 3.1). Для противоточных абсорберов X*к
=f(Yн
). По графику максимально возможная концентрация ацетона в воде при условиях абсорбции составляет X*к
max
=0,408 . .

Т.к. в реальном процессе абсорбции используется не минимальный расход поглотителя, а несколько больший (для ускорения процесса), то необходимо пересчитать минимальный расход поглотителя на рабочий расход L
с учетом коэффициента избытка поглотителя [4]
 , (3.11) , (3.11)
где a ‑ коэффициент избытка поглотителя, принимаем равным 1,5.
С увеличением расхода поглотителя (т. е. с увеличением коэффициента избытка поглотителя) снижаются допустимые скорости газа в аппарате, по которым находят его диаметр. Поэтому следует выбирать такое соотношение между размерами абсорбционного аппарата и расходом поглотителя, при котором размеры аппарата будут оптимальными [5].
 . .
Для определения рабочей концентрации служит уравнение [2]:
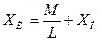 , (3.12) , (3.12)
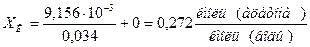
2.2.4
Построение рабочей линии абсорбции ацетона и определение числа единиц переноса
По полученным значениям концентраций строится график (рисунок 3.2)
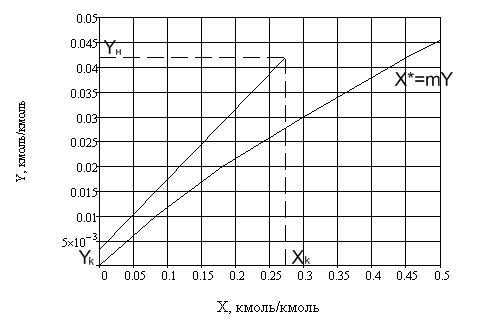
Рисунок 3.2 - X – Y диаграмма при давлении р = 0.25 МПа
3.3 Определение рабочей скорости газа и диаметра аппарата
Для начала необходимо выбрать тип тарелки. Большое разнообразие тарельчатых контактных устройств затрудняет выбор оптимальной конструкции тарелки. Выберем колпачковый тип тарелки, а именно тарелки колпачковые однопоточные стальные разборные типа ТСК-Р, так как они могут работать при большой нагрузке по жидкости, у них большая область устойчивой работы, большая эффективность, они обладают лёгкостью пуска и установки.
Для колпачковых тарелок предельно допустимую скорость рекомендуется рассчитывать по формуле:
 (3.13) (3.13)
где ρx
и ρy
–плотности жидкой и газообразной фазы соответственно, ρx
= 998 кг/м3
[3];
dk
-диаметр колпачка ,м;
hk
-расстояние от верхнего края колпачка до вышерасположенной тарелки , м.
Плотность газообразной фазы найдем по формуле [3]:
 , (3.14) , (3.14)
где Мсм
– молярная масса парогазовой смеси, кг/кмоль;
Т0
, р0
– соответственно температура и давление при нормальных условиях (Т0
= 273К, р0
= 1,013∙105
Па);
t – температура абсорбции равная 26 °С по заданию;
р – давление в абсорбере равное 0,25 МПа.
Молярная масса парогазовой смеси рассчитывается по формуле [3]:
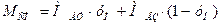 , (3.15) , (3.15)
где Мац
– молярная масса ацетона равная 58 кг/кмоль;
Мвз
– молярная масса воздуха равная 29 кг/кмоль;
ун
‑ исходная концентрация ацетона в газовой смеси, 
Получаем,
Мсм
= 58∙0,04 + 29∙(1-0,04) = 30,16 кг/кмоль,
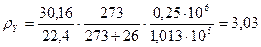 кг/м3
. кг/м3
.
Диаметр колпачка dk
и расстояние от верхнего края колпачка до вышерасположенной тарелки hk
выберем согласно [6] таблица 24.2: dk
= 0,1 м, hk
= 0.3м.
Тогда предельно допустимая скорость будет равна:
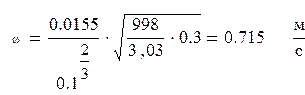
Рабочая скорость будет равна [1]
 , м/с , м/с
Диаметр абсорбера находим из уравнения расхода [1]:
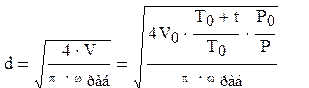 , (3.16) , (3.16)
где V – объёмный расход газа при условиях в абсорбере, м3
/с. Отсюда

Выбираем стандартный диаметр обечайки абсорбера dст
=2,4 м. При этом действительная рабочая скорость газа в абсорбере [1]
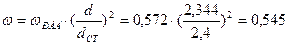 , м/с. , м/с.
3.4 Высота светлого слоя жидкости
Высоту светлого слоя жидкости на тарелке h0
находим из соотношения[1]:
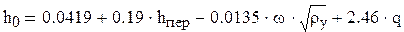 , (3.17) , (3.17)
где hпер
– высота переливной перегородки, согласно [6] hпер
= 0,05 м;
q – линейная плотность орошения, м3
/(м∙с).
Рассчитаем линейную плотность орошения q [1]:
q = Q/Lc
, (3.18)
где Q – объёмный расход жидкости м3
/с;
Lс
– периметр слива, Lс
= 1,775 м [6].
Объемный расход жидкости равен:
 , (3.19) , (3.19)
где L – молярный расход чистого поглотителя, кмоль/с;
ρх
– плотность чистого поглотителя при температуре абсорбции, кг/м3
;
Мв
– молярная масса воды равная 18 кг/кмоль.
 , м3
/с , м3
/с
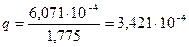 ,м3
/(м∙с) ,м3
/(м∙с)
Подставив получим:
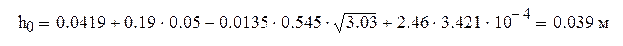
3.5 Расчёт коэффициентов массоотдачи
Коэффициент массопередачи определяют по уравнению аддитивности фазовых диффузионных сопротивлений[1] :
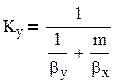 , (3.20) , (3.20)
где βх
и βу
– коэффициенты массоотдачи, отнесённые к единице рабочей площади тарелки соответственно для жидкой и газовой фаз, кг/(м2
·с);
m – коэффициент распределения,
m = 0,1006 кмоль воды/кмоль воздуха.
Для жидкой фазы коэффициент массоотдачи [1]:
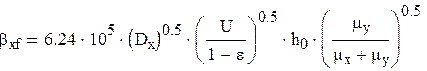 , (3.21) , (3.21)
где Dx
– коэффициент молекулярной диффузии распределяемого компонента в жидкости, м2
/с;
ε – газосодержание барботажного слоя,м3
/м3
;
U – плотность орошения;
μх
– вязкость воды, равная 1 мПа∙с по [3] рисунок V;
μу
- вязкость воздуха, равная 0,018 мПа∙с по [3] рисунок VI;
h0
– высота светлого слоя жидкости, м.
Плотность орошения равна [1]:
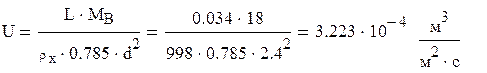
где L – молярный расход поглотителя, кмоль/с;
МВ
– молярная масса воды, кг/кмоль;
ρx
– плотность воды, при температуре абсорбции, кг/м3
.
Согласно [1] рассчитаем Dх
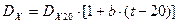 , (3.22) , (3.22)
где Dx
20
– коэффициент диффузии в жидкости при t = 20°C, м2
/с;
b – температурный коэффициент;
t – температура абсорбции.
Коэффициент диффузии в жидкости при 20°С можно вычислить по приближенной формуле [1]:
 , (3.23) , (3.23)
где А, В – коэффициенты ассоциации, учитывающие отклонения от нормы в поведении растворенного вещества и растворителя. Согласно [4] c.660 А= 1, для воды В = 4,7;
υац
и υв
– мольные объемы ацетона и воды соответственно при нормальной температуре кипения, (υв
= 18,9 см3
/моль, υац
=74 см3
/моль, [3]);
μX
– вязкость жидкости при 20 °С, равная 1 мПа∙с.
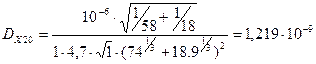 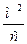 . .
Температурный коэффициент b определяем по формуле [1]:
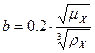 , (3.24) , (3.24)
где μx
и ρx
принимаем при температуре 20 °С [3]
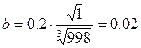 . .
При температуре абсорбции 26 °С коэффициент диффузии DX
будет равен:
 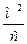 . .
Газосодержание барботажного слоя определяем из соотношения [1]
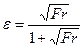 , (3.25) , (3.25)
где Fr – критерий Фруда.
Критерий Фруда рассчитывается по формуле [1]:
 , (3.26) , (3.26)
где wТ
– скорость газа в рабочем сечении тарелки, м/с;
h0
– высота газожидкостного слоя, м;
g = 9.81 м2
/с.
Скорость газа в рабочем сечении тарелки найдем по [1]
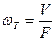 , (3.27) , (3.27)
где V – объемный расход газовой смеси при условиях абсорбции, м3
/с;
F – рабочее сечение тарелки, м2
. В соответствии с [6] таблица 5.2 для колпачковых тарелок типа ТСК-Р с диаметром колонны 2,4 м F = 3,48 м2
.
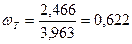 м/с м/с
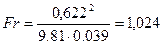 . .
Тогда газосодержание барботажного слоя:
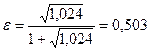  . .
Подставим все полученные значения в формулу (3.21)
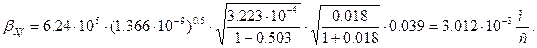
Для газовой фазы коэффициент массоотдачи [1]:
 , (3.28) , (3.28)
где Fс
– свободное сечение тарелки, равное 12,3% или 0,123 по [1] Приложение 5.2;
Dy
– коэффициент диффузии в газовой фазе, м2
/с;
wт
– скорость газа в рабочем сечении тарелки, м/с.
Коэффициент диффузии ацетона в воздухе при атмосферном давлении и температуре t = 0°С по [8] D0У
= 1,09∙10-5
м2
/с. Пересчитаем это значение на условия абсорбции по формуле [3]:
 , (3.29) , (3.29)
где Т0
, р0
– соответственно температура и давление при нормальных условиях (Т0
= 273К, р0
= 1,013∙105
Па);
Т – температура абсорбции, К;
р – абсолютное давление в абсорбере, Па.
Подставив , получим:
 м2
/с. м2
/с.
Подставив данные в формулу (3.), получаем
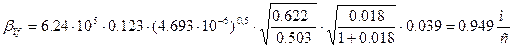
Переведём коэффициенты массоотдачи в нужную размерность
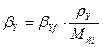  , (3.30) , (3.30)
где Мсм
– молярная масса парогазовой смеси, кг/кмоль;
ρу
– плотность газовой смеси, кг/м3
.
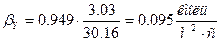 . .
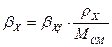  , (3.31) , (3.31)
где Мсм
– молярная масса жидкой смеси, кг/кмоль;
ρx
– плотность жидкости, кг/м3
.
Молярная масса жидкой смеси равна:
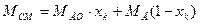 , (3.32) , (3.32)
где хк
– абсолютная мольная доля ацетона в воде, кмоль ацетона/кмоль смеси.
Произведем перерасчет из относительных в абсолютные мольные доли[1]:
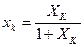 , (3.33) , (3.33)
 кмоль ацетона/кмоль ж. смеси. кмоль ацетона/кмоль ж. смеси.
 . .
Тогда коэффициент массотдачи:
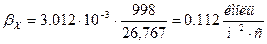 . .
Рассчитаем теперь коэффициент массопередачи по формуле (3.20)
 . .
3.6 Поверхность массопередачи и высота абсорбера
Поверхность массопередачи в абсорбере рассчитывается по уравнению:
 , (3.34) , (3.34)
где М - молярный расход ацетона, кмоль/с;
КУ
– коэффициент массопередачи, кмоль/м2
∙с;
ΔYср
– движущая сила процесса, кмоль/кмоль.
Движущая сила может быть выражена в единицах концентрации как жидкой, так и газовой фаз. Принимая модель идеального вытеснения в потоках обеих фаз, определим движущую силу в единицах концентраций газовой фазы:
 (3.35) (3.35)
где ΔYб
и ΔYм
– большая и меньшая движущие силы на входе потоков в абсорбер и на выходе из него, кмоль ацетона/кмоль воздуха.

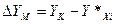 (3.36) (3.36)
где YХн
и YХк
– концентрация ацетона в газе, равновесные с концентрациями в жидкой фазе (поглотителе) соответственно на входе в абсорбер и на выходе из него:
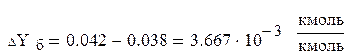
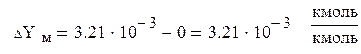

Отсюда

Тогда требуемое число тарелок [1]
 , (3.37) , (3.37)
где Fраб
- рабочее сечение тарелки, которое равно [6] 3,48 м2
.

Принимаем n = 10 тарелок.
3.7 Выбор расстояния между тарелками и определение высоты абсорбера
Расстояние между тарелками принимают равным или несколько большим суммы высот барботажного слоя (пены) hп
и сепарационного пространства hc
[1]:
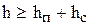 , (3.38) , (3.38)
Высоту пены рассчитаем по формуле
 , (3.39) , (3.39)
Подставив получим
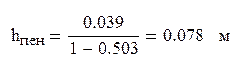
Высоту сепарационного пространства рассчитываем исходя из допустимого брызгоуноса с тарелки, принимаемого равным 0.1 кг жидкости на 1 кг газа используя формулу [1]:
 , (3.40) , (3.40)
где Е – масса жидкости уносимой с 1 м2
рабочей площади сечения колонны, кг/м2
·с;
σ – поверхностное натяжение, σ = 72.8 мН/м [3].
Согласно графику для определения уноса на колпачковых тарелках [1] рисунок 5.5:
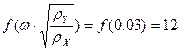
Из (3.) выразим hс
:
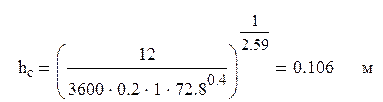
Найдём расстояние между тарелками по формуле (3.41)
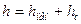 , (3.41) , (3.41)
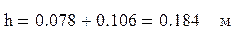
Принимаем h = 0.3 м [6] таблица 24.2.
Рассчитаем высоту тарельчатой части по формуле (3.42):
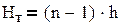 , (3.42) , (3.42)
Подставив значения, получим
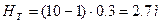 . .
Расстояние между нижней тарелкой и днищем абсорбера примем по [7] равным 5 м, а расстояние между верхней тарелкой и крышкой абсорбера 1.6, тогда общая высота абсорбера :

3.
8 Гидравлическое сопротивление тарелок абсорбера
Гидравлическое сопротивление тарелок абсорбера определяют по формуле [2]:
 (3.43) (3.43)
Полное гидравлическое сопротивление одной тарелки складывается из трёх слагаемых:
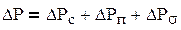 , (3.44) , (3.44)
Гидравлическое сопротивление сухой тарелки
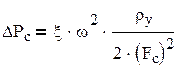 , (3.45) , (3.45)
где ξ – коэффициент сопротивления сухой тарелки, для колпачковой тарелки ξ = 4,5 [6];
FC
– относительное свободное сечение для прохода газа по тарелке, для колпачковой тарелки FC
=0,123 [1].
Получим:
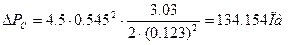
Гидравлическое сопротивление газожидкостного слоя (пены) на тарелке [9] c. 229:
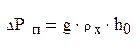 (3.46) (3.46)
где g – ускорение свободного падения, м2
/с;
ρх
– плотность жидкости, кг/м3
;
h0
– высота светлого слоя жидкости, м.
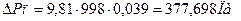
Гидравлическое сопротивление, обусловленное силами поверхностного натяжения [2]:
 (3.47) (3.47)
где σ – поверхностное натяжение жидкости, равное 72,8∙10-3
Н/м;
dЭ
– эквивалентный диаметр щелей, через которые газ проходит в жидкость на тарелке, м.
Рассчитаем эквивалентный диаметр для треугольной прорези со сторонами 16.55 мм, 16.55 мм, 14 мм [6].
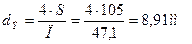
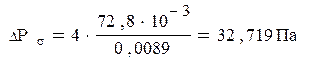
Тогда полное гидравлическое сопротивление

Гидравлическое сопротивление всех тарелок абсорбера
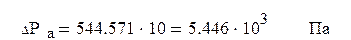
3.9 Определение диаметра штуцеров
Для расчетов диаметров штуцеров служит следующее уравнение [1] с.16:
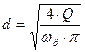 , (3.48) , (3.48)
где wр
‑ рекомендуемая среднерасходная скорость перемещения среды в штуцере,м/с;
Q – объемный расход, м3
/с.
Руководствуясь [1] примем ωp
газа
=15 м/с, ωp
жидк.
=0.8 м/с.
Так как давление в абсорбере небольшое, согласно рекомендациям [12] выберем штуцера ОСТ 26 – 1404.
Объемный расход жидкой смеси равен:
 (3.49) (3.49)
где L – мольный расход поглотителя, кмоль/с;
М – молярная масса поглотителя, кг/кмоль;
ρ – плотность поглотителя при температуре абсорбции, кг/м3
.

Определяем диаметр основных технических штуцеров для подвода и отвода жидкой смеси:
 . .
Примем штуцер с Dy
=60 мм.
Определяем диаметр основных технических штуцеров для подвода и отвода газовой смеси.
 . .
Примем штуцер с Dу
=500 мм.
|